题目内容
元素性质呈现周期性变化的根本原因是( )
| A、原子半径呈周期性变化 |
| B、元素化合价呈周期性变化 |
| C、电子层数逐渐增加 |
| D、元素原子的核外电子排布呈周期性变化 |
考点:元素周期律的实质
专题:
分析:根据随原子序数的递增,原子的结构呈现周期性的变化而引起元素的性质的周期性变化来解答.
解答:
解:A、因元素的原子半径是元素的性质,不能解释元素性质的周期性变化,故A错误;
B、因元素的化合价属于元素的性质,则不能解释元素性质的周期性变化,故B错误;
C、电子层数逐渐增加,则不能解释元素性质的周期性变化,故C错误;
D、因原子的核外电子排布中电子层数和最外层电子数都随原子序数的递增而呈现周期性变化,则引起元素的性质的周期性变化,故D正确;
故选:D.
B、因元素的化合价属于元素的性质,则不能解释元素性质的周期性变化,故B错误;
C、电子层数逐渐增加,则不能解释元素性质的周期性变化,故C错误;
D、因原子的核外电子排布中电子层数和最外层电子数都随原子序数的递增而呈现周期性变化,则引起元素的性质的周期性变化,故D正确;
故选:D.
点评:本题考查元素周期律的实质,明确原子的结构与性质的关系、元素的性质有哪些是解答的关键,并注意不能用元素本身的性质来解释元素性质的周期性变化.

练习册系列答案
相关题目
下列过程或现象与盐类水解无关的是( )
| A、可用碳酸钠与醋酸制取少量二氧化碳 |
| B、泡沫灭火器用碳酸氢钠溶液和硫酸铝溶液,使用时只需将其混合就可产生大量二氧化碳的泡沫 |
| C、厨房中常用碳酸钠溶液洗涤餐具上的油污 |
| D、实验室盛放碳酸钠溶液的试剂瓶必须用橡胶塞而不能用玻璃塞 |
与铁相似,金属锡能与盐酸反应生成氯化亚锡(SnCl2),氯化亚锡又能被氯化铁氧化为氯化锡(SnCl4).则下列有关粒子氧化性和还原性强弱的比较中,正确的是( )
| A、氧化性:Sn4+<Sn2+ |
| B、氧化性:Fe3+<Sn4+ |
| C、还原性:Fe2+<Sn2+ |
| D、还原性:Fe<Sn |
对于排布在2s轨道上的电子,不能确定的是( )
| A、电子所在的电子层 |
| B、电子的自旋方向 |
| C、电子云的形状 |
| D、电子云的伸展方向 |
在相同条件下,若A容器中的氢气与B容器中的氨气(NH3)所含原子数相等,则两个容器的体积比为( )
| A、1:2 | B、1:3 |
| C、2:3 | D、2:1 |
下列离子方程式正确的是( )
| A、金属钠与水反应:Na+2H2O=Na++2OH-+H2↑ |
| B、金属铝投入NaOH溶液中:Al+2OH-=AlO2-+H2↑ |
| C、稀硝酸中加入过量铁粉:Fe+4H++NO3-=Fe3++NO↑+2H2O |
| D、FeCl2酸性溶液放在空气中变质:4Fe2++4H++O2=4Fe3++2H2O |
反应Fe(s)+CO2(g)?FeO(s)+CO(g),700℃时平衡常数为1.47,900℃时平衡常数为2.15.下列说法正确的是( )
| A、升高温度该反应的正反应速率增大,逆反应速率减小 | ||
B、该反应的化学平衡常数表达式为K=
| ||
| C、绝热容器中进行该反应,温度不再变化,则达到化学平衡状态 | ||
| D、该反应的正反应是放热反应 |
 根据如图所示装置回答问题:
根据如图所示装置回答问题: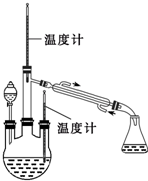 肼是重要的化工原料.某探究小组利用下列反应制取水合肼(N2H4?H2O).CO(NH2)+2NaOH+NaClO=Na2CO3+N2H4?H2O+NaCl
肼是重要的化工原料.某探究小组利用下列反应制取水合肼(N2H4?H2O).CO(NH2)+2NaOH+NaClO=Na2CO3+N2H4?H2O+NaCl