题目内容
下列过程或现象与盐类水解无关的是( )
| A、可用碳酸钠与醋酸制取少量二氧化碳 |
| B、泡沫灭火器用碳酸氢钠溶液和硫酸铝溶液,使用时只需将其混合就可产生大量二氧化碳的泡沫 |
| C、厨房中常用碳酸钠溶液洗涤餐具上的油污 |
| D、实验室盛放碳酸钠溶液的试剂瓶必须用橡胶塞而不能用玻璃塞 |
考点:盐类水解的应用
专题:盐类的水解专题
分析:A、是利用酸性强弱分析;
B、泡沫灭火器用碳酸氢钠溶液和硫酸铝溶液,混合后发生双水解反应;
C、碳酸钠溶液水解显碱性,油脂在碱溶液中水解生成易溶于水的物质易于洗涤;
D、碳酸钠溶液水解显碱性,和玻璃中的二氧化硅反应生成硅酸钠,是矿物胶,瓶口和瓶塞粘结在一起不易打开;
B、泡沫灭火器用碳酸氢钠溶液和硫酸铝溶液,混合后发生双水解反应;
C、碳酸钠溶液水解显碱性,油脂在碱溶液中水解生成易溶于水的物质易于洗涤;
D、碳酸钠溶液水解显碱性,和玻璃中的二氧化硅反应生成硅酸钠,是矿物胶,瓶口和瓶塞粘结在一起不易打开;
解答:
解:A、醋酸酸性比碳酸弱,可用碳酸钠与醋酸制取少量二氧化碳,与盐类水解无关,故A符合;
B、泡沫灭火器用碳酸氢钠溶液和硫酸铝溶液,混合后铝离子和碳酸氢根离子发生双水解生成二氧化碳和氢氧化铝沉淀,故B不符合;
C、碳酸钠溶液水解显碱性,油脂在碱溶液中水解生成易溶于水的物质易于洗涤,和盐类水解有关,故C不符合;
D、碳酸钠溶液水解显碱性,和玻璃中的二氧化硅反应生成硅酸钠,是矿物胶,瓶口和瓶塞粘结在一起不易打开,和盐类水解有关,故D不符合;
故选A.
B、泡沫灭火器用碳酸氢钠溶液和硫酸铝溶液,混合后铝离子和碳酸氢根离子发生双水解生成二氧化碳和氢氧化铝沉淀,故B不符合;
C、碳酸钠溶液水解显碱性,油脂在碱溶液中水解生成易溶于水的物质易于洗涤,和盐类水解有关,故C不符合;
D、碳酸钠溶液水解显碱性,和玻璃中的二氧化硅反应生成硅酸钠,是矿物胶,瓶口和瓶塞粘结在一起不易打开,和盐类水解有关,故D不符合;
故选A.
点评:本题考查了盐类水解的分析应用,主要是影响因素分析判断,掌握基础是关键,题目难度中等.

练习册系列答案
 超能学典应用题题卡系列答案
超能学典应用题题卡系列答案
相关题目
在373K 时,把0.5mol N2O4气体通入体积为5L的密闭容器中发生反应:N2O4(g)?2NO2(g).反应进行到2s时,NO2的浓度为0.02mol?L-1.在60s时,体系已达到平衡,此时容器内压强为反应前的1.6倍.下列说法不正确的是( )
| A、平衡时,化学平衡常数K=1.8 |
| B、平衡时,N2O4的转化率为60% |
| C、前2s,N2O4的平均反应速率为0.005mol?L-1?s-1 |
| D、在2s时,体系内压强为反应前的1.1倍 |
关于Na2O2的叙述正确的是(NA表示阿伏伽德罗常数)( )
| A、7.8g Na2O2含有的共价键数为0.2NA |
| B、7.8 g Na2S与Na2O2的混合物,含离子总数为0.3 NA |
| C、7.8g Na2O2与足量的CO2充分反应,转移的电数为0.2NA |
| D、0.2 mol Na被完全氧化生成7.8g Na2O2,转移电子的数目为0.4NA |
2011年,在欧洲一些国家发现饲料被污染,导致畜禽类制品及乳制品不能食用,经测定饲料中含有剧毒物质二恶英,其结构为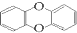 ,已知它的二氯代物有10种,则其六氯代物有( )
,已知它的二氯代物有10种,则其六氯代物有( )
 ,已知它的二氯代物有10种,则其六氯代物有( )
,已知它的二氯代物有10种,则其六氯代物有( )| A、5种 | B、11种 |
| C、10种 | D、5种 |
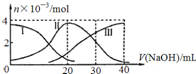 常温下,向20mL 0.2mol/L H2A溶液中滴加0.2mol/L NaOH溶液.有关微粒的物质的量变化如图,下列说法正确的是( )
常温下,向20mL 0.2mol/L H2A溶液中滴加0.2mol/L NaOH溶液.有关微粒的物质的量变化如图,下列说法正确的是( )| A、滴加过程中当溶液呈中性时,V(NaOH)≥20mL |
| B、当V(NaOH)=30mL时,则有:2c(Na+)=3c(A2-)+3c(HA-) |
| C、H 2A在水中的电离方程式是:H 2A→H++HA-; HA-?H++A2- |
| D、当V(NaOH)=20mL时,则有:c(Na+)>c(HA-)>c(H+)>c(A2-)>c(OH-) |
在下列叙述中,不能证明醋酸是弱电解质的是( )
| A、室温下,0.1mol?L-1的CH3COONa溶液的pH=8 |
| B、醋酸与CaCO3反应有气体生成 |
| C、室温下,0.1mol?L-1的CH3COOH溶液的pH=3 |
| D、醋酸中加水后,溶液的pH升高 |
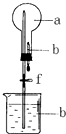 如图装置中,干燥烧瓶中盛满某种气体,烧杯和滴管内盛放某种溶液.挤压滴管的胶头,下列与实验事实不相符的是( )
如图装置中,干燥烧瓶中盛满某种气体,烧杯和滴管内盛放某种溶液.挤压滴管的胶头,下列与实验事实不相符的是( )| A、若a为NO,b为NaOH溶液,可出现无色喷泉 |
| B、若a为HCl,b为AgNO3溶液,可出现白色喷泉 |
| C、若a为CO2,b为NaOH溶液,可出现无色喷泉 |
| D、若a为NH3,b为水(预先滴入少量酚酞溶液),可出现红色喷泉 |
下列与金属腐蚀有关的说法中,不正确的是( )
| A、钢铁在潮湿空气中生锈属于电化学腐蚀 |
| B、电化学腐蚀一般可分为吸氧腐蚀和析氢腐蚀 |
| C、金属腐蚀的本质是金属原子失去电子被氧化的过程 |
| D、铝具有很强的抗腐蚀能力,是因为其不易与氧气发生反应 |
元素性质呈现周期性变化的根本原因是( )
| A、原子半径呈周期性变化 |
| B、元素化合价呈周期性变化 |
| C、电子层数逐渐增加 |
| D、元素原子的核外电子排布呈周期性变化 |