题目内容
18.某强酸性反应体系中,反应物和生成物共六种物质:PbO2、PbSO4 (难溶盐)、Pb(MnO4)2(高锰酸铅强电解质)、H2O、X(水溶液呈无色)、H2SO4,已知X是一种盐,且0.1molX在该反应中应失去3.01×1023个电子.下列说法中不正确的是( )| A. | 若有9.8gH2SO4参加反应,则转移电子的物质的量为1mol | |
| B. | 该反应的化学方程式为:5PbO2+2MnSO4+2H2SO4═Pb(MnO4)2+4PbSO4+2H2O | |
| C. | Pb(MnO4)2既是氧化产物又是还原产物 | |
| D. | X是MnSO4 |
分析 X是一种硫酸盐,且0.1mol X在该反应中失去0.5mol 电子,即1molX在该反应中失去5mol电子,根据元素守恒知,该元素是锰元素,生成物中锰元素是+7价,则X中锰元素显+2价,所以X是MnSO4,该反应方程式为:2MnSO4+5PbO2+2H2SO4=Pb(MnO4)2+4PbSO4+2H2O,以此解答该题.
解答 解:X是一种硫酸盐,且0.1mol X在该反应中失去0.5mol 电子,即1molX在该反应中失去5mol电子,根据元素守恒知,该元素是锰元素,生成物中锰元素是+7价,则X中锰元素显+2价,所以X是MnSO4,该反应方程式为:2MnSO4+5PbO2+2H2SO4=Pb(MnO4)2+4PbSO4+2H2O,
A.9.8g H2SO4参加反应,则n(H2SO4)=0.1mol,由方程式可知:2MnSO4~Pb(MnO4)2~2H2SO4 ~10mol电子,则0.1molH2SO4反应转移0.5mol电子,故A错误;
B.由以上分析可知反应的方程式为5PbO2+2MnSO4+2H2SO4═Pb(MnO4)2+4PbSO4+2H2O,故B正确;
C.反应中Mn元素化合价升高,Pb元素化合价降低,则Pb(MnO4)2既是氧化产物又是还原产物,故C正确;
D.由以上分析可知X是MnSO4,故D正确.
故选A.
点评 本题考查氧化还原反应及计算,为高频考点,把握元素的化合价变化及电子守恒为解答的关键,注意浓盐酸与PbO2发生的氧化还原反应,题目难度中等.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
9.工业上从废铅酸电池的铅膏回收铅的过程中,可用碳酸盐溶液与铅膏(主要成分为PbSO4)发生反应:PbSO4(s)+CO32-(aq)?PbCO3(s)+SO42-(aq).Ksp (PbCO3)=1.5×10-13,Ksp (PbSO4)=1.8×10-8某课题组用PbSO4为原料模拟该过程,探究上述反应的实验条件及固体产物的成分.
(1)计算上述反应的平衡常数:K=1.2×105.
(2)加入足量NaHCO3溶液也可实现该转化,写出离子方程式2HCO3-+PbSO4=SO42-+PbCO3+H2O+CO2↑
(3)查阅文献:上述反应还可能生成碱式碳酸铅[2PbCO3•Pb(OH)2],它和PbCO3受热都易分解成PbO.该课题组对固体产物(不考虑PbSO4)的成分提出如下假设,
假设一:全部为2PbCO3•Pb(OH)2;
假设二:全部为PbCO3;
假设三:2PbCO3•Pb(OH)2 和PbCO3的混合物
为验证假设一是否成立,课题组进行如下研究.
①你是否同意该同学的结论,并简述理由不同意.若为假设三,有同样的现象.
②如果不同意,请提出改进意见将气体依次通过足量的浓硫酸和澄清石灰水,并分别测量增重的质量,通过计算确定H元素和C元素的物质的量之比.若n(C):n(H)=1:1,则为假设一,若n(c):n(H)>1:1,则为假设三.
(1)计算上述反应的平衡常数:K=1.2×105.
(2)加入足量NaHCO3溶液也可实现该转化,写出离子方程式2HCO3-+PbSO4=SO42-+PbCO3+H2O+CO2↑
(3)查阅文献:上述反应还可能生成碱式碳酸铅[2PbCO3•Pb(OH)2],它和PbCO3受热都易分解成PbO.该课题组对固体产物(不考虑PbSO4)的成分提出如下假设,
假设一:全部为2PbCO3•Pb(OH)2;
假设二:全部为PbCO3;
假设三:2PbCO3•Pb(OH)2 和PbCO3的混合物
为验证假设一是否成立,课题组进行如下研究.
| 实验步骤 | 实验现象和结论 |
| 取一定量样品充分干燥,然后将样品加热分解,将产生的气体依次通过盛有无水硫酸铜的干燥管和盛有澄清石灰水的洗气瓶. | 无水硫酸铜变蓝色,澄清石灰水变浑浊 说明样品全部是2PbCO3•Pb(OH)2 |
②如果不同意,请提出改进意见将气体依次通过足量的浓硫酸和澄清石灰水,并分别测量增重的质量,通过计算确定H元素和C元素的物质的量之比.若n(C):n(H)=1:1,则为假设一,若n(c):n(H)>1:1,则为假设三.
6.某溶液中含有大量的下列离子:Mg2+、NO3-、K+和M离子,经测定Mg2+、NO3-、K+离子的物质的量浓度之比为2:4:1,则M离子可能是下列中的( )
| A. | H+ | B. | SO42- | C. | OH- | D. | Na+ |
13. 等质量的铁与过量的盐酸在不同的实验条件下进行反应,测定在不同时间t产生氢气体积V的数据,根据数据绘制得下图,则曲线a、b、c、d所对应的实验组别可能是( )
等质量的铁与过量的盐酸在不同的实验条件下进行反应,测定在不同时间t产生氢气体积V的数据,根据数据绘制得下图,则曲线a、b、c、d所对应的实验组别可能是( )
 等质量的铁与过量的盐酸在不同的实验条件下进行反应,测定在不同时间t产生氢气体积V的数据,根据数据绘制得下图,则曲线a、b、c、d所对应的实验组别可能是( )
等质量的铁与过量的盐酸在不同的实验条件下进行反应,测定在不同时间t产生氢气体积V的数据,根据数据绘制得下图,则曲线a、b、c、d所对应的实验组别可能是( )| 组别 | c(HCl)(mol•L-1) | 温度(℃) | 状态 |
| 1 | 2.0 | 25 | 块状 |
| 2 | 2.5 | 30 | 块状 |
| 3 | 2.5 | 50 | 粉末状 |
| 4 | 2.5 | 30 | 粉末状 |
| A. | 4-3-2-1 | B. | 1-2-3-4 | C. | 3-2-4-1 | D. | 3-4-2-1 |
10.氢氟酸是一种弱酸,已知25℃时:
①HF(aq)+OH-(aq)═F-(aq)+H2O(l)△H=-67.7kJ•mol-1
②H+(aq)+OH-(aq)═H2O(l)△H=-57.3kJ•mol-1
在20mL 0.1mol/L氢氟酸中加V mL 0.1mol/L NaOH溶液.下列说法错误的是( )
①HF(aq)+OH-(aq)═F-(aq)+H2O(l)△H=-67.7kJ•mol-1
②H+(aq)+OH-(aq)═H2O(l)△H=-57.3kJ•mol-1
在20mL 0.1mol/L氢氟酸中加V mL 0.1mol/L NaOH溶液.下列说法错误的是( )
| A. | 氢氟酸电离的热化学方程式为:HF(aq)?F-(aq)+H+(aq)△H=-10.4 kJ•mol-1 | |
| B. | 当V=20时,溶液中:c(OH-)=c(H+)+c(HF) | |
| C. | 当V=20时,溶液中:c(F-)<c(Na+)=0.1 mol/L | |
| D. | 当V=20时,溶液中水的电离程度最大(忽略溶液温度的变化) |
8.下列关于化学平衡的叙述,正确的是( )
| A. | 化学平衡是动态平衡 | |
| B. | 各反应物的浓度等于各生成物的浓度 | |
| C. | 正逆反应速率为零 | |
| D. | 反应物和生成物的浓度不再改变,反应已停止 |
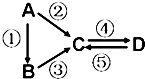 A、B、C、D均为中学化学常见的纯净物,A是单质.它们之间有如下的反应关系:
A、B、C、D均为中学化学常见的纯净物,A是单质.它们之间有如下的反应关系: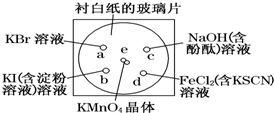 化学实验的微型化可有效地减少污染,实现化学实验绿色化的要求.某学生按下列操作做一个实验:在一块下衬白纸的玻璃片的不同位置分别滴加浓度为0.1mol/L的KBr、KI(含淀粉溶液)、NaOH(含酚酞)、FeCl2(含KSCN)溶液各1滴,每种液滴彼此分开,围成半径小于表面皿的圆形(如下图所示),在圆心处放置2粒芝麻粒大小的KMnO4晶体,向KMnO4晶体滴加一滴浓盐酸,再立即将表面皿盖好.(已知:2KMnO4+16HCl(浓)═2KCl+2MnCl2+5Cl2↑+8H2O
化学实验的微型化可有效地减少污染,实现化学实验绿色化的要求.某学生按下列操作做一个实验:在一块下衬白纸的玻璃片的不同位置分别滴加浓度为0.1mol/L的KBr、KI(含淀粉溶液)、NaOH(含酚酞)、FeCl2(含KSCN)溶液各1滴,每种液滴彼此分开,围成半径小于表面皿的圆形(如下图所示),在圆心处放置2粒芝麻粒大小的KMnO4晶体,向KMnO4晶体滴加一滴浓盐酸,再立即将表面皿盖好.(已知:2KMnO4+16HCl(浓)═2KCl+2MnCl2+5Cl2↑+8H2O