题目内容
除去下列物质中少量杂质的方法正确的是( )
| A、除去Fe2(SO4)3溶液中混有的Fe SO4:加入足量新制氯水 |
| B、除去FeCl2溶液中混有的FeCl3:加入足量铁粉,过滤 |
| C、铝粉中的镁粉,加入足量氢氧化钠溶液,过滤 |
| D、除去Cu粉中混有的CuO:加适量稀硝酸后,过滤、洗涤 |
考点:物质的分离、提纯和除杂
专题:化学实验基本操作
分析:A.氯水中有氯离子;
B.铁离子能和铁反应生成亚铁离子;
C.铝可与氢氧化钠溶液反应;
D.二者均与硝酸反应.
B.铁离子能和铁反应生成亚铁离子;
C.铝可与氢氧化钠溶液反应;
D.二者均与硝酸反应.
解答:
解:A.氯水中有氯离子,加入氯水引入了新的杂质,故A错误;
B.因为铁离子能和铁反应生成亚铁离子,故可用铁除去FeCl2溶液中的少量氯化铁,故B正确;
C.镁和氢氧化钠不反应,而铝可与氢氧化钠溶液反应,将原物质除掉,故C错误;
D.二者均与硝酸反应,不能除杂,应加稀盐酸后,过滤、洗涤来除杂,故D错误.
故选B.
B.因为铁离子能和铁反应生成亚铁离子,故可用铁除去FeCl2溶液中的少量氯化铁,故B正确;
C.镁和氢氧化钠不反应,而铝可与氢氧化钠溶液反应,将原物质除掉,故C错误;
D.二者均与硝酸反应,不能除杂,应加稀盐酸后,过滤、洗涤来除杂,故D错误.
故选B.
点评:本题考查物质分离、提纯的方法和应用,为高频考点,把握物质的性质及性质差异为解答的关键,注意发生的反应及除杂的原则,题目难度不大.

练习册系列答案
相关题目
下列叙述正确的是(NA为阿伏伽德罗常数)( )
| A、标况下,22.4L苯的分子数为NA |
| B、10.0mL 18mol/L的浓硫酸中氢离子数为0.36NA |
| C、6.4gS6与S8的混合物中所含S原子数一定为0.2NA |
| D、标准状况下,22.4L氯气与足量氢氧化钠溶液反应转移的电子数为2NA |
下列小实验设计肯定合理的是( )
| A、用AgNO3鉴别工业盐(亚硝酸钠)和食盐二种溶液 |
| B、海带中碘元素提取时氧化滤液中的I-时应加入过量氯水 |
| C、将3-4个火柴头浸于水中,片刻后取少量溶液于试管中,加AgNO3溶液、稀硝酸和NaNO2溶液,若出现白色沉淀,说明含有氯元素 |
| D、溶质的溶解度越大,溶液的浓度越高,溶剂的蒸发速度越快,溶液的冷却速度越快,析出的晶体就越细小 |
下列说法正确的是(NA为阿伏加德罗常数)( )
| A、标准状况下,1L苯完全燃烧所生成的气态产物的分子数为6/22.4NA |
| B、1 mol甲基(-CH3)所含的电子总数为9NA |
| C、1 mol聚乙烯含有的原子数目为6NA |
| D、12 g金刚石中含有C-C键的个数为NA |
 拟除虫菊酯是一类高效、低毒、对昆虫具有强烈触杀作用的杀虫剂,其中对光稳定的溴氰菊酯的结构简式如图,下列对该化合物叙述正确的是( )
拟除虫菊酯是一类高效、低毒、对昆虫具有强烈触杀作用的杀虫剂,其中对光稳定的溴氰菊酯的结构简式如图,下列对该化合物叙述正确的是( )| A、属于芳香烃 |
| B、在一定条件下可以发生加成反应 |
| C、在碱性条件下不水解 |
| D、属于卤代烃 |
下列过程中,没有明显实验现象的是( )
| A、向饱和碳酸钠溶液通入CO2气体 |
| B、少量过氧化钠投入AlCl3溶液 |
| C、向碳酸氢钠溶液中滴加氢氧化钠溶液 |
| D、向Fe(NO3)2溶液中滴加稀硫酸 |
某离子化合物的晶胞如图所示立体结构,晶胞是整个晶体中最基本的重复单位.小黑球表示阳离子,小白球表示阴离子,该离子化合物中,阴、阳离子个数比是( )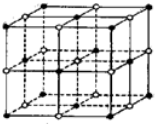

| A、1:8 | B、1:4 |
| C、1:2 | D、1:1 |
相同状态下,10体积A2气体和20体积B2气体化合成20体积气体C,则C的化学式为( )
| A、AB |
| B、A2B |
| C、AB3 |
| D、AB2 |