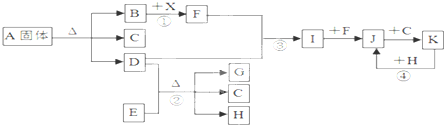
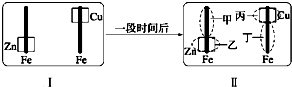
题目内容
下列说法正确的是(NA为阿伏加德罗常数)( )
| A、标准状况下,1L苯完全燃烧所生成的气态产物的分子数为6/22.4NA |
| B、1 mol甲基(-CH3)所含的电子总数为9NA |
| C、1 mol聚乙烯含有的原子数目为6NA |
| D、12 g金刚石中含有C-C键的个数为NA |
考点:阿伏加德罗常数
专题:阿伏加德罗常数和阿伏加德罗定律
分析:A.根据标准状况下,苯的状态不是气体进行判断;
B.甲基是甲烷失去一个H原子后剩余的部分,其中化学键表示一个未成对电子;
C.根据聚乙烯的分子式来解答;
D.每个C原子与其他4个C原子共用4个C-C键,相当于每个C原子占有4×
=2个C-C键.
B.甲基是甲烷失去一个H原子后剩余的部分,其中化学键表示一个未成对电子;
C.根据聚乙烯的分子式来解答;
D.每个C原子与其他4个C原子共用4个C-C键,相当于每个C原子占有4×
| 1 |
| 2 |
解答:
解:A.标准状况下,苯不是气体,不能使用标况下的气体摩尔体积计算苯的物质的量,故A错误;
B.甲基是甲烷失去一个H原子后剩余的部分,所以一个甲基中的电子数是9,则1mol甲基(一CH3)所含的电子数应为9NA,故B正确;
C.聚乙烯分子式: ,可知1mol聚乙烯含原子数目为6nNA,故C错误;
,可知1mol聚乙烯含原子数目为6nNA,故C错误;
D.每个C原子与其他4个C原子共用4个C-C键,相当于每个C原子占有4×
=2个C-C键,1mol金刚石含2molC-C键,故D错误.
故选B.
B.甲基是甲烷失去一个H原子后剩余的部分,所以一个甲基中的电子数是9,则1mol甲基(一CH3)所含的电子数应为9NA,故B正确;
C.聚乙烯分子式:
 ,可知1mol聚乙烯含原子数目为6nNA,故C错误;
,可知1mol聚乙烯含原子数目为6nNA,故C错误;D.每个C原子与其他4个C原子共用4个C-C键,相当于每个C原子占有4×
| 1 |
| 2 |
故选B.
点评:本题考查阿佛加德罗常数,难度不大,注意每个C原子与其他4个C原子共用4个C-C键及石墨中的成键即可解答.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
以下对实验操作的说法正确的是( )
| A、配制FeCl3溶液时,应将FeCl3溶解在适量的盐酸中 |
| B、进行焰色反应时,所用铂丝先用NaOH溶液洗涤并充分灼烧 |
| C、用CCl4萃取碘水中的I2时,有机层从分液漏斗的下端放出 |
| D、酸碱中和滴定时,锥形瓶需用待测液润洗2遍,再加入待测液 |
下列说法正确的是( )
| A、炔烃可以使溴的四氯化碳溶液褪色,不能使酸性高锰酸钾溶液褪色 |
| B、某有机物燃烧只生成等物质的量的CO2和H2O,则此有机物的组成为CnH2n |
| C、鉴定溴乙烷中溴原子的存在的实验操作是:向溴乙烷中加入NaOH溶液,加热后加入AgNO3溶液 |
D、在分子 中,处于同一平面上的碳原子最多可能有12个 中,处于同一平面上的碳原子最多可能有12个 |
除去下列物质中少量杂质的方法正确的是( )
| A、除去Fe2(SO4)3溶液中混有的Fe SO4:加入足量新制氯水 |
| B、除去FeCl2溶液中混有的FeCl3:加入足量铁粉,过滤 |
| C、铝粉中的镁粉,加入足量氢氧化钠溶液,过滤 |
| D、除去Cu粉中混有的CuO:加适量稀硝酸后,过滤、洗涤 |
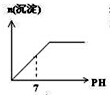
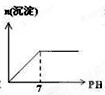
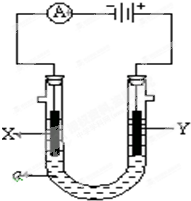 电解原理在化学工业中有广泛应用.如图表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连.请回答以下问题:
电解原理在化学工业中有广泛应用.如图表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连.请回答以下问题: