题目内容
16.空气污染已成为人类社会面临的重大威胁.下列气体中,会造成空气污染的是( )| A. | N2 | B. | O2 | C. | CO2 | D. | SO2 |
分析 根据N2为空气的主要成分,不是污染物,而Cl2、SO2、NO2都有毒,排放在空气中,造成空气污染,以此来解答.
解答 解:N2、O2、CO2为空气的主要成分,无毒,不会造成空气污染,SO2有毒,排放在空气中,造成空气污染,
故选D.
点评 本题考查有毒气体和环境污染,为高频考点,侧重于化学与环境的考查,有利于培养学生良好的科学素养,提高学习的积极性,熟悉常见的空气污染物即可解答,题目较简单.

练习册系列答案
 学业测评一课一测系列答案
学业测评一课一测系列答案
相关题目
7.共价键都有键能之说,键能是指拆开1mol共价键所需要吸收的能量或生成1mol共价键所能够放出的能量.如H-H键的键能是指1mol H2分子变成2mol H原子需要吸收436KJ的能量或2mol H原子变成1mol H2分子能够放出436KJ的能量.
(1)已知H-Cl键的键能为431.4kJ/mol,下列关于键能的叙述正确的是AD
A.每生成1molH-Cl键放出431.4kJ能量
B.每生成1molH-Cl键吸收431.4kJ能量
C.每拆开1molH-Cl键放出431.4kJ能量
D.每拆开1mol H-Cl键吸收431.4kJ能量
(2)参考表中的数据,判断下列分子受热时最稳定的是A
A、HF B、HCI C、HBr D、H2
(3)能用键能大小解释的是A
A、氮气的化学性质比氧气稳定
B、常温常压下,溴呈液态,碘呈固态
C、稀有气体一般很难发生化学反应
D、硝酸易挥发而硫酸难挥发.
(1)已知H-Cl键的键能为431.4kJ/mol,下列关于键能的叙述正确的是AD
A.每生成1molH-Cl键放出431.4kJ能量
B.每生成1molH-Cl键吸收431.4kJ能量
C.每拆开1molH-Cl键放出431.4kJ能量
D.每拆开1mol H-Cl键吸收431.4kJ能量
(2)参考表中的数据,判断下列分子受热时最稳定的是A
| 化学键 | H-H | H-F | H-Cl | H-Br |
| 键能kJ/mol | 436 | 565 | 431 | 368 |
(3)能用键能大小解释的是A
A、氮气的化学性质比氧气稳定
B、常温常压下,溴呈液态,碘呈固态
C、稀有气体一般很难发生化学反应
D、硝酸易挥发而硫酸难挥发.
4.下列分子式表示的各物质中,属于烃的是( )
| A. | C2H6O | B. | C6H6 | C. | HCN | D. | CO(NH2)2 |
11.填表:
| 发展阶段 | 原子结构模型 | 重要科学家 |
| 1 | 近代原子论 | |
| 2 | 汤姆生 | |
| 3 | 原子行星模型 |
1.检验铵盐的方法是将待检物取出少量放在试管中,然后( )
| A. | 加热,用湿润的红色石蕊试纸在试管口观察现象 | |
| B. | 加水溶解,用红色石蕊试纸测其溶液的酸碱性 | |
| C. | 加强碱溶液,加热,滴入酚酞试液,观察溶液颜色 | |
| D. | 加苛性钠溶液,加热,用湿润的红色石蕊试纸在试管口进行检验 |
8.5个碳的烷烃的同分异构体共有( )
| A. | 1种 | B. | 2种 | C. | 3种 | D. | 4种 |
6.设NA是阿伏加德罗常数的数值,下列说法正确的是( )
| A. | 1.8gNH${\;}_{4}^{+}$和2.3gNa+所含的电子数均为NA | |
| B. | 0.4molCu与0.8molHNO3(稀)反应,转移电子数为0.8NA | |
| C. | 3.2gCu与足量的HNO3(浓)反应生成的气体分子数为0.1NA | |
| D. | 1molCl2与足量的铁反应,转移的电子数为3NA |
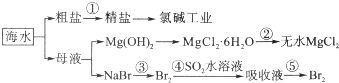
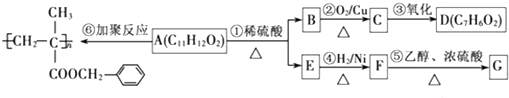
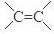 、-COOH;F的名称2-甲基丙酸(系统命名法命名).
、-COOH;F的名称2-甲基丙酸(系统命名法命名).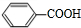 .
.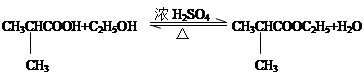 .⑤的反应类型是酯化反应(或取代反应).
.⑤的反应类型是酯化反应(或取代反应).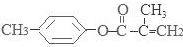 .
.