题目内容
18.下列混合物可以用分液漏斗分离的是( )| A. | 溴乙烷和水 | B. | 汽油和苯 | C. | 乙醇和水 | D. | 溴苯和苯 |
分析 根据分液漏斗可以将互不相溶的两层液体分开,则分析选项中物质的溶解性即可.
解答 解:A.溴乙烷和水不溶,能用分液漏斗进行分离,故A正确;
B.汽油和苯互溶,不能用分液漏斗进行分离,故B错误;
C.乙醇和水互溶,不能用分液漏斗进行分离,故C错误;
D.溴苯和苯互溶,不能用分液漏斗进行分离,故D错误.
故选A.
点评 本题考查了物质的分离和提纯,难度不大,注意分液漏斗能分离的物质必须是互不相溶的液体.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
8.具有下列电子层结构的原子,则下列有关比较中正确的是( )
①3p轨道上只有一对成对电子的原子
②外围电子构型为2s22p5的原子
③其3p轨道为半充满的原子
④正三价的阳离子结构与氖相同的原子.
①3p轨道上只有一对成对电子的原子
②外围电子构型为2s22p5的原子
③其3p轨道为半充满的原子
④正三价的阳离子结构与氖相同的原子.
| A. | 第一电离能:②>③>①>④ | B. | 原子半径:④>③>②>① | ||
| C. | 电负性:②>③>①>④ | D. | 最高正化合价:②>③>①>④ |
9.下列有关有机化合物的说法正确的是( )
| A. | 用水可以区分苯和CCl4 | |
| B. | 有机物分子中都存在碳碳单键 | |
| C. | 做银镜反应实验后的试管内壁附有银,可用稀盐酸清洗 | |
| D. | 检验乙醇消去后的产物乙烯,可将气体直接通入酸性高锰酸钾溶液中 |
13.下列说法中,不正确的是( )
| A. | 乙醇与金属钠反应时,是乙醇分子中羟基中的O-H键断裂 | |
| B. | 检验乙醇中是否含有水,可加入少量无水硫酸铜,若变蓝则含水 | |
| C. | 向待测液中加入饱和碳酸钠溶液鉴别乙酸、乙酸乙酯、乙醇 | |
| D. | 向苯和苯酚混合溶液中滴加过量浓溴水除去混合溶液中的苯酚 |
3.某主族元素X的电子式为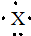 ,则该元素组成的以下物质中,化学式肯定错误的是( )
,则该元素组成的以下物质中,化学式肯定错误的是( )
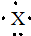 ,则该元素组成的以下物质中,化学式肯定错误的是( )
,则该元素组成的以下物质中,化学式肯定错误的是( )| A. | 含氧酸的化学式可能为HXO3 | B. | 含氧酸的化学式可能为H3XO4 | ||
| C. | 气态氢化物化学式为XH5 | D. | 最高价氧化物的化学式为X2O5 |
10.一定条件下,对于可逆反应X(g)+3Y(g)?2Z(g),若X、Y、Z的起始浓度分别为c1、c2、c3(均不为零),达到平衡时,X、Y、Z的浓度分别为0.1mol/L、0.3mol/L、0.08mol/L,则下列判断正确的是( )
| A. | c1:c2=3:1 | |
| B. | 平衡时,Y和Z的生成速率之比为2:3 | |
| C. | X、Y的转化率相等 | |
| D. | c1的取值范围为0 mol/L≤c1≤0.14 mol/L |
7.X、Y、Z、W是原子序数依次增大的四种短周期元素,甲、乙、丙、丁、戊是由其中的两种或三种元素组成的化合物,己是由Z元素形成的单质.已知:甲+乙=丁+己,甲+丙=戊+己; 丁溶液为短周期元素中最高价氧化物对应水化物中碱性最强的物质.下列说法正确的是( )
| A. | 原子半径:W>Z>Y>X | |
| B. | Y元素在周期表中的位置为第三周期第ⅣA族 | |
| C. | 1mol甲与足量的乙完全反应共转移了1mol电子 | |
| D. | 甲、乙、丙、丁、戊、己中含有的共价键的物质只有乙、丙、己 |
8.某有机物M的结构简式如图所示: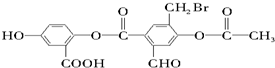 下列说法正确的是( )
下列说法正确的是( )
 下列说法正确的是( )
下列说法正确的是( )| A. | 1 mol M最多能与10×22.4 L氢气(标准状况)发生加成反应 | |
| B. | 1 mol M最多能与2 mol Na HCO3反应 | |
| C. | 1 mol M最多能与5 mol NaOH反应 | |
| D. | 1 mol M最多能与2 mol Na反应 |
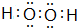 .
.