题目内容
3.某主族元素X的电子式为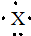 ,则该元素组成的以下物质中,化学式肯定错误的是( )
,则该元素组成的以下物质中,化学式肯定错误的是( )| A. | 含氧酸的化学式可能为HXO3 | B. | 含氧酸的化学式可能为H3XO4 | ||
| C. | 气态氢化物化学式为XH5 | D. | 最高价氧化物的化学式为X2O5 |
分析 根据电子式可知原子最外层电子数5,其最高化合价应为+5价,最低化合价为-3价,以此进行判断.
解答 解:某主族元素X的电子式为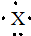 ,根据电子式可知原子最外层电子数5,其最高化合价应为+5价,最低化合价为-3价,则
,根据电子式可知原子最外层电子数5,其最高化合价应为+5价,最低化合价为-3价,则
A.最高化合价为+5价,如为N元素,则含氧酸分子式为HRO3,故A正确;
B.最高化合价为+5价,如为P元素,则含氧酸分子式为H3RO4,故B正确;
C.最低化合价为-3价,则气态氢化物分子式为RH3,故C错误.
D.最高化合价为+5价,则最高价氧化物分子式为R2O5,故D正确;
故选C.
点评 本题考查元素对应化学式的推断,题目难度不大,本题注意根据电子式推断元素的可能种类以及最高化合价以及最低化合价.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
13.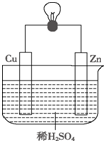 如图是Zn和Cu形成的原电池,某实验兴趣小组做完实验后,做了如下记录,其中描述合理的是( )
如图是Zn和Cu形成的原电池,某实验兴趣小组做完实验后,做了如下记录,其中描述合理的是( )
①Zn为正极,Cu为负极;
②H+向负极移动;
③电子流动方向:从Zn经外电路流向Cu;
④Cu极上有H2产生;
⑤正极的电极反应式为:Zn-2e-═Zn2+
⑥若有1mol电子流过导线,则产生H2为0.5mol.
 如图是Zn和Cu形成的原电池,某实验兴趣小组做完实验后,做了如下记录,其中描述合理的是( )
如图是Zn和Cu形成的原电池,某实验兴趣小组做完实验后,做了如下记录,其中描述合理的是( )①Zn为正极,Cu为负极;
②H+向负极移动;
③电子流动方向:从Zn经外电路流向Cu;
④Cu极上有H2产生;
⑤正极的电极反应式为:Zn-2e-═Zn2+
⑥若有1mol电子流过导线,则产生H2为0.5mol.
| A. | ①②③ | B. | ③④⑥ | C. | ④⑤⑥ | D. | ②③④ |
14.一定条件下,在密闭容器中,能表示反应X(g)+2Y(g)═2Z(g)一定达到化学平衡状态的是( )
①X、Y、Z的物质的量之比是1:2:2
②X、Y、Z的浓度不再发生变化
③容器中的压强不再发生变化
④单位时间内生成n molZ,同时生成2n mol Y
⑤容器中平均相对分子质量不再发生变化
⑥v(X,正)=2v(Z,逆)
①X、Y、Z的物质的量之比是1:2:2
②X、Y、Z的浓度不再发生变化
③容器中的压强不再发生变化
④单位时间内生成n molZ,同时生成2n mol Y
⑤容器中平均相对分子质量不再发生变化
⑥v(X,正)=2v(Z,逆)
| A. | ②③④ | B. | ①②④ | C. | ②③⑤ | D. | ③④⑥ |
18.下列混合物可以用分液漏斗分离的是( )
| A. | 溴乙烷和水 | B. | 汽油和苯 | C. | 乙醇和水 | D. | 溴苯和苯 |
12.食盐(NaCl)是生活中常用的调味品,HCl是胃酸的主要成分,下列关于这两种物质的说法正确的是( )
| A. | 炒菜时放入食盐并不破坏NaCl中的离子键 | |
| B. | HCl的电子式是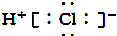 | |
| C. | HCl是共价化合物,但溶于水时电离出H+和Cl- | |
| D. | NaCl熔化时破坏共价键 |
13.戊醇的分子式为C5H120,若由戊烯与水发生加成反应生成戊醇,则生成的戊醇的结构最多有(不考虑立体异构 )( )
| A. | 5种 | B. | 7种 | C. | 8种 | D. | 9种 |
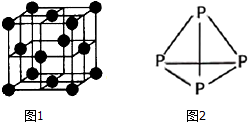 氨是重要的化工原料,用途广泛.
氨是重要的化工原料,用途广泛.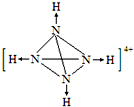 .
.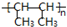 .
. .
.