题目内容
19.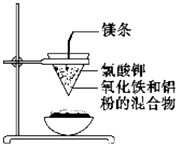 如图所示:用两张圆形滤纸分别折叠成漏斗状,套在一起,使四周都有四层.把内层滤纸取出,在底部剪一个小孔,用水润湿,再跟另一纸漏斗套在一起,架在铁圈上,下面放置一盛沙的蒸发皿.把5g干燥的氧化铁粉末和2g铝粉混合均匀,放在纸漏斗中,上面加少量氯酸钾并在混合物中间插一根镁条,用小木条点燃镁条.观察发生的现象.通过以上实验信息,回答下列问题:
如图所示:用两张圆形滤纸分别折叠成漏斗状,套在一起,使四周都有四层.把内层滤纸取出,在底部剪一个小孔,用水润湿,再跟另一纸漏斗套在一起,架在铁圈上,下面放置一盛沙的蒸发皿.把5g干燥的氧化铁粉末和2g铝粉混合均匀,放在纸漏斗中,上面加少量氯酸钾并在混合物中间插一根镁条,用小木条点燃镁条.观察发生的现象.通过以上实验信息,回答下列问题:(1)写出该反应的化学方程式:Fe2O3+2Al$\frac{\underline{\;高温\;}}{\;}$Al2O3+2Fe,该反应称为铝热反应.
(2)选出该实验的实验现象(填写在横线上):①②③④.
①镁条剧烈燃烧
②放出大量的热,并发出耀眼的光芒,火星四射
③纸漏斗的下部被烧穿
④有红热状态的液珠落入蒸发皿内的细沙上,液珠冷却后变为黑色固体
(3)写出各物质的作用:蒸发皿盛沙:为防止溅落物炸裂蒸发皿;镁条:引燃剂;氯酸钾:助燃剂.
分析 (1)氧化铁和铝粉在高温条件下发生铝热反应生成铁和氧化铝;该反应称为铝热反应;
(2)根据铝热反应的反应现象“反应放出大量的热,并发出耀眼的光,纸漏斗的下部被烧穿,有熔融物落入沙中”等现象进行判断;
(3)反应生成的熔融物温度很高,容易使蒸发皿炸裂;镁条作引燃剂;氯酸钾作助燃剂,据此进行解答.
解答 解:(1)氧化铁和铝粉在高温条件下发生铝热反应生成铁和氧化铝,反应的化学方程式为:Fe2O3+2Al$\frac{\underline{\;高温\;}}{\;}$Al2O3+2Fe;该反应为铝热反应,
故答案为:Fe2O3+2Al$\frac{\underline{\;高温\;}}{\;}$Al2O3+2Fe;铝热;
(2)该反应在高温条件下进行,反应的现象有:镁条剧烈燃烧、放出大量的热,并发出耀眼的光芒,火星四射、纸漏斗的下部被烧穿、有红热状态的液珠落入蒸发皿内的细沙上,液珠冷却后变为黑色固体,所以①②③④都正确,
故答案为:①②③④;
(3)铝热反应中,为了防止溅落物炸裂蒸发皿,需要在蒸发皿中盛放沙;该反应需要在高温下进行,镁条作引燃剂,氯酸钾在反应物起到助燃剂的作用,使反应产生高温,引发铝热反应,
故答案为:为防止溅落物炸裂蒸发皿;引燃剂;助燃剂.
点评 本题考查了铝热反应原理及反应现象、操作方法等知识,题目难度中等,要求掌握铝热反应发生原理、反应装置及正确的操作方法,明确铝热反应的现象,试题培养了学生灵活应用所学知识的能力.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
9.下列各组物质中,都是极性分子的一组是( )
| A. | NH3 H2O | B. | CO2 HCl | C. | NO H2 | D. | CH4 Br2 |
14.10ml浓度为1mol/L的盐酸与过量的锌粉反应,若加入适量的下列溶液,能减慢反应速率但又不影响氢气生成总量的是( )
①K2SO4 ②CH3COONa ③CuSO4 ④Na2SO4.
①K2SO4 ②CH3COONa ③CuSO4 ④Na2SO4.
| A. | ①③ | B. | ②④ | C. | ①②④ | D. | ③④ |
4.设NA表示阿伏伽德罗常数的值,下列说法正确的是( )
| A. | 17gOH-中所含电子数为10NA | |
| B. | Na2O2固体中的阳离子和阴离子个数比是1:1 | |
| C. | 9g重水(${\;}_{1}^{2}$D2O)所含有的电子数为5NA | |
| D. | 在标准状况下,11.2L氖气含有NA个氖原子 |
11.Mg-AgCl电池是一种以海水为电解质溶液的水激活电池.下列叙述错误的是( )
| A. | 负极反应式为Mg-2e-=Mg2+ | |
| B. | 电池放电时Cl-由正极向负极迁移 | |
| C. | 正极反应式为Ag++e-=Ag | |
| D. | 负极会发生副反应Mg+2H2O=Mg(OH)2+H2↑ |
8.已知J、L、M、R、T是原子序数依次增大的短周期主族元素,J、R在周期表中的相对位置如下表;J元素最低负化合价的绝对值与其原子最外层电子数相等;M是地壳中含量最多的金属元素.请回答下列问题:
(1)M的离子结构示意图为 ;
;
(2)元素T在周期表中的位置是第三周期ⅦA.
(3)L的最简单气态氢化物甲的水溶液显碱性.
①在微电子工业中,甲的水溶液可作刻蚀剂H2O2的清除剂,所发生反应的产物不污染环境,其化学方程式为2NH3•H2O+3H2O2═N2↑+8H2O或2NH3+3H2O2═N2↑+6H2O.
②一定条件下,甲在固定体积的密闭容器中发生分解反应(△H>0)并达平衡后,仅改变下表中反应条件x,该平衡体系中随x递增y递减的是ac(选填序号).
(4)由J、R形成的液态化合物JR2 0.2mol在O2中完全燃烧,生成两种气态氧化物,298K时放出热量215kJ.该反应的热化学方程式为CS2(l)+3O2(g)=CO2(g)+2SO2(g)△H=-1075KJ/mol.
| J | ||||
| R |
 ;
;(2)元素T在周期表中的位置是第三周期ⅦA.
(3)L的最简单气态氢化物甲的水溶液显碱性.
①在微电子工业中,甲的水溶液可作刻蚀剂H2O2的清除剂,所发生反应的产物不污染环境,其化学方程式为2NH3•H2O+3H2O2═N2↑+8H2O或2NH3+3H2O2═N2↑+6H2O.
②一定条件下,甲在固定体积的密闭容器中发生分解反应(△H>0)并达平衡后,仅改变下表中反应条件x,该平衡体系中随x递增y递减的是ac(选填序号).
| 选项 | a | b | c | d |
| x | 温度 | 温度 | 加入H2的物质的量 | 加入甲的物质的量 |
| y | 甲的物质的量 | 平衡常数K | 甲的转化率 | 生成物物质的量总和 |
 .
.