题目内容
2.一定温度下的恒容容器中,能标志某可逆反应A(s)+2B(g)?C(g)+D(g)已达平衡状态的是( )| A. | 混合气体的压强不随时间变化而变化 | |
| B. | 气体总物质的量不随时间变化而变化 | |
| C. | 2v正(B)=v逆(D) | |
| D. | 混合气体的密度保持不变 |
分析 恒温恒容条件下,反应A(s)+2B(g)?C(g)+D(g)已达平衡状态,说明正逆反应速率相等,反应体系中各组分的浓度不再变化;注意该反应中气体的体积不变,反应物B是固体.
解答 解:A、由于反应方程式中气体的体积不变,容器容积不变,所以压强始终不变,因此压强不变,无法判断正逆反应速率是否相等,故A错误;
B、反应两边气体的化学计量数之和相等,气体的物质的量始终不变,所以气体总物质的量不随时间变化而变化,不能判断是否达到平衡状态,故B错误;
C、v正(B)=2v逆(D),表明D的正逆反应速率相同,反应达到平衡状态,但是2v正(B)=v逆(D)不满足B和D的化学计量数关系,正逆反应速率不相等,反应一定没有达到平衡状态,故C错误;
D、A为固体,体积不变,气体质量发生改变什么屁话发生移动,所以密度不变说明反应达到了平衡状态,故D正确;
故选:D.
点评 本题考查了化学平衡状态的判断,题目难度不大,注意化学反应达到平衡状态,正逆反应速率一定相等,反应体系中各组分浓度不再变化.

练习册系列答案
 习题精选系列答案
习题精选系列答案
相关题目
6.某实验报告记录了如下数据,其中数据合理的是( )
| A. | 用10mL量筒量取5.26mL稀硫酸 | |
| B. | 用托盘天平称量11.7g氧化铜粉末 | |
| C. | 用广泛pH试纸测得某溶液的pH为3.5 | |
| D. | 用酸式滴定管量取10.5mL盐酸溶液 |
13.下列电子式正确的是( )
| A. | 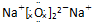 | B. | 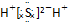 | C. | 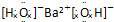 | D. | 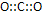 |
17.甲烷分子是以碳原子为中心的正四面体结构,而不是正方形的平面结构,理由是( )
| A. | CH3Cl只有一种结构 | B. | CH2Cl2只有一种结构 | ||
| C. | CHCl3只有一种结构 | D. | CH4中含有4个C-H极性键 |
7.已知:SeO2+4KI+4HNO3═Se+2I2+4KNO3+2H2O,对于该氧化还原反应,下列说法错误的是( )
| A. | 硝酸在该反应中起酸性和氧化性作用 | |
| B. | 生成0.5molSe,转移电子数为2NA | |
| C. | I2是氧化产物 | |
| D. | 氧化剂和还原剂的物质的量之比为1:4 |
12.在一密闭容器中,一定条件下发生反应A+3B?2C,在10秒内反应物A的浓度由1mol/L降到0.6mol/L,则用B浓度的变化表示的该反应在这段时间内的平均反应速率为( )
| A. | 0.04 mol/(L•s) | B. | 0.12 mol/(L•s) | C. | 0.4 mol/(L•s) | D. | 1.2 mol/(L•s) |
 .
.