题目内容
12.在一密闭容器中,一定条件下发生反应A+3B?2C,在10秒内反应物A的浓度由1mol/L降到0.6mol/L,则用B浓度的变化表示的该反应在这段时间内的平均反应速率为( )| A. | 0.04 mol/(L•s) | B. | 0.12 mol/(L•s) | C. | 0.4 mol/(L•s) | D. | 1.2 mol/(L•s) |
分析 化学反应速率表示单位时间内浓度的变化量,利用v=$\frac{△c}{△t}$计算出v(A),再根据计量数之比等于速率比求算v(B).
解答 解:10秒内,用A浓度的变化表示平均反应速率为v=$\frac{△c}{△t}$=$\frac{1mol/L-0.6mol/L}{10s}$=0.04mol/(L•s),则v(B)=3v(A)=0.12mol/(L•s).
故选B.
点评 本题考查化学反应速率的计算,难度不大,注意对基础知识的理解和反应速率之比等于化学方程式计量数之比的计算.

练习册系列答案
相关题目
2.一定温度下的恒容容器中,能标志某可逆反应A(s)+2B(g)?C(g)+D(g)已达平衡状态的是( )
| A. | 混合气体的压强不随时间变化而变化 | |
| B. | 气体总物质的量不随时间变化而变化 | |
| C. | 2v正(B)=v逆(D) | |
| D. | 混合气体的密度保持不变 |
17.根据表中信息判断,下列选项错误的是( )
| 序号 | 反应物 | 产物 |
| ① | KMnO4、H2O2、H2SO4 | K2SO4、MnSO4、H2O、O2 |
| ② | Cl2、FeBr2 | FeCl3、Br2 |
| ③ | KMnO4、HCl | Cl2、MnCl2 |
| A. | 第①组反应中,H2O2作还原剂 | |
| B. | 第②组反应中,Cl2与FeBr2的物质的量之比可能为3:2 | |
| C. | 第③组反应中,每生成1mol Cl2转移电子2mol | |
| D. | 从三个反应可以得出:氧化性由强到弱顺序为MnO4->Fe3+>Cl2>Br2 |
4.等物质的量的下列有机物,充分燃烧耗氧量最大的是( )
| A. | C3H8 | B. | C2H6O | C. | C4H8O | D. | C4H8O2 |
3.设NA为阿伏加德罗常数的数值,下列说法正确的是( )
| A. | 常温下,44gCO2含有NA个C原子 | |
| B. | 1 L0.1mol•L-1Na2S溶液中含有0.1NA个S2- | |
| C. | 0.1mol Na与足量O2反应,转移0.2NA个电子 | |
| D. | 标准状况下,22.4L的CCl4含有4NA个Cl原子 |
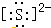


 .
.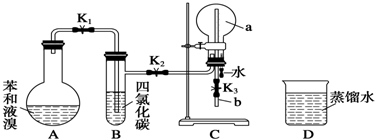
 ,能证明凯库勒观点错误的实验现象是C中产生“喷泉”现象.
,能证明凯库勒观点错误的实验现象是C中产生“喷泉”现象.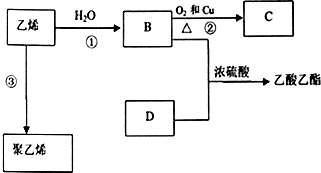 已知乙烯能发生以下转化:
已知乙烯能发生以下转化: .
.