题目内容
17.甲烷分子是以碳原子为中心的正四面体结构,而不是正方形的平面结构,理由是( )| A. | CH3Cl只有一种结构 | B. | CH2Cl2只有一种结构 | ||
| C. | CHCl3只有一种结构 | D. | CH4中含有4个C-H极性键 |
分析 若甲烷是正四面体,则CH2Cl2只有一种结构,而若甲烷为正方形的平面结构,则CH2Cl2有两种结构,据此分析.
解答 解:A、若甲烷是正四面体,则CH3Cl只有一种结构,而若甲烷为正方形的平面结构,则CH3Cl也只有一种结构,故CH3Cl只有一种结构不能说明甲烷是哪种构型,故A错误;
B、若甲烷是正四面体,则CH2Cl2只有一种结构,而若甲烷为正方形的平面结构,则CH2Cl2有两种结构,而事实是CH2Cl2只有一种结构,故可以说明甲烷为正四面体结构而非平面结构,故B正确;
C、若甲烷是正四面体,则CHCl3只有一种结构,而若甲烷为正方形的平面结构,则CHCl3也只有一种结构,故CHCl3只有一种结构,不鞥说明甲烷为正四面体结构而非平面结构,故C错误;
D、无论甲烷为正四面体结构还是平面结构,甲烷中均含4条C-H极性键,故甲烷中含4条C-H极性键不可以说明甲烷为正四面体结构而非平面结构,故D错误.
故选B.
点评 本题考查常见有机化合物的结构,题目难度中等,注意CH2Cl2只代表一种物质,可以证明甲烷分子是空间正四面体结构,而不是平面正方形结构.

练习册系列答案
相关题目
8.某元素原子序数为85,下面关于该元素说法不正确的是( )
| A. | 它的银盐不溶于水 | |
| B. | 它的氢化物很不稳定 | |
| C. | 它的单质是白色固体 | |
| D. | 该元素位于元素周期表第六周期、第十七列 |
5.R、M、T、G、J为原子序数依次递增的同一短周期主族元素,下列说法一定正确的是(m、n均为正整数)( )
| A. | 若G的最高价氧化物水化物为强酸,则J一定是活泼非金属元素 | |
| B. | HnJOm为强酸,则G是位于VA族以后的活泼非金属元素 | |
| C. | 若T的最低化合价为-3,则G的最高正化合价为+6 | |
| D. | 若M的最高正化合价为+4,则五种元素不一定都是非金属元素 |
12.如图实验装置图正确的是( )
| A. | 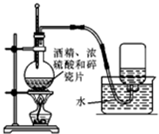 实验室制乙烯 | B. | 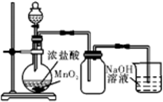 实验室制氯气 | ||
| C. | 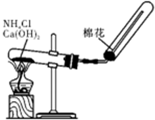 实验室制氨气 | D. |  实验室制乙酸乙酯 |
2.一定温度下的恒容容器中,能标志某可逆反应A(s)+2B(g)?C(g)+D(g)已达平衡状态的是( )
| A. | 混合气体的压强不随时间变化而变化 | |
| B. | 气体总物质的量不随时间变化而变化 | |
| C. | 2v正(B)=v逆(D) | |
| D. | 混合气体的密度保持不变 |
9.分类是学习和研究化学的一种重要方法,下列分类合理的是( )
| A. | Fe3O4和Na2O2都属于碱性氧化物 | B. | KOH和Na2CO3都属于碱 | ||
| C. | NaHSO4和NaHCO3都属于酸式盐 | D. | Na2O和Al2O3都属于碱性氧化物 |
6.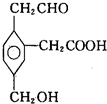 某有机物的结构简式如图所示,在一定条件下对于下列反应:
某有机物的结构简式如图所示,在一定条件下对于下列反应:
①加成、②水解、③酯化、④氧化、⑤中和、⑥消去,其中该物质可能发生的是( )
 某有机物的结构简式如图所示,在一定条件下对于下列反应:
某有机物的结构简式如图所示,在一定条件下对于下列反应:①加成、②水解、③酯化、④氧化、⑤中和、⑥消去,其中该物质可能发生的是( )
| A. | ②③④ | B. | ①③④⑤ | C. | ①③⑤⑥ | D. | ②③④⑤⑥ |
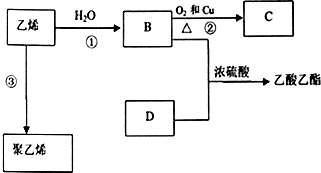 已知乙烯能发生以下转化:
已知乙烯能发生以下转化: .
.