题目内容
11.在下列物质中:①CO2 ②KCl ③CaBr2 ④O2 ⑤NH4Cl ⑥Ca(OH)2 ⑦N2 ⑧HBr ⑨NH3 ⑩Na2O2(1)只有非极性键的是④⑦;
(2)只有极性键的是①⑧⑨;
(3)只有离子键的是③;
(4)既有离子键,也有非极性键的是⑩;
(5)属于共价化合物的是①⑧⑨.
分析 一般来说,活泼金属和活泼非金属元素之间易形成离子键,不同非金属元素之间易形成极性键,同种非金属元素之间易形成非极性键,含有离子键的化合物是离子化合物,只含共价键的化合物是共价化合物,以此来解答.
解答 解:①CO2中只含C=O极性共价键,为共价化合物;
②KCl只含离子键,为离子化合物;
③CaBr2只含离子键,为离子化合物;
④O2中只含非极性共价键,为单质;
⑤NH4Cl中含离子键和N-H极性共价键,为离子化合物;
⑥Ca(OH)2中含离子键和O-H极性共价键,为离子化合物;
⑦N2中只含非极性共价键,为单质;
⑧HBr中只含H-Br极性共价键,为共价化合物;
⑨NH3中只含H-N极性共价键,为共价化合物;
⑩Na2O2中含离子键和O-O非极性共价键,为离子化合物,
(1)只有非极性键的是④⑦,故答案为:④⑦;
(2)只有极性键的是①⑧⑨,故答案为:①⑧⑨;
(3)只有离子键的是③,故答案为:③;
(4)既有离子键,也有非极性键的是⑩,故答案为:⑩;
(5)属于共价化合物的是①⑧⑨,故答案为:①⑧⑨.
点评 本题考查化学键及物质分类,为高频考点,把握化学键的形成及判断的一般规律为解答的关键,注意含离子键的化合物一定为离子化合物,题目难度不大.

练习册系列答案
 优等生题库系列答案
优等生题库系列答案 53天天练系列答案
53天天练系列答案
相关题目
1.绿色化学又称环境友好化学,它的主要特点之一是:提高原子的利用率,使原料中所有的原子全部转化到产品中,实现“零排放”.下列反应符合绿色化学这一特点的是( )
| A. | 工业冶铁Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2 | |
| B. | 用生石灰制熟石灰CaO+H2O=Ca(OH)2 | |
| C. | 实验室制取二氧化碳CaCO3+2HCl=CaCl2+H2O+CO2↑ | |
| D. | 实验室制取氢气Zn+H2SO4=ZnSO4+H2↑ |
2.一定温度下的恒容容器中,能标志某可逆反应A(s)+2B(g)?C(g)+D(g)已达平衡状态的是( )
| A. | 混合气体的压强不随时间变化而变化 | |
| B. | 气体总物质的量不随时间变化而变化 | |
| C. | 2v正(B)=v逆(D) | |
| D. | 混合气体的密度保持不变 |
19.下列化学实验事实及其解释不正确的是( )
| A. | 钠保存在煤油中,是因为煤油不与钠发生反应,钠比煤油密度大,煤油可以使钠隔绝空气和水蒸气 | |
| B. | 用洁净的玻璃管向包有Na2O2的脱脂棉吹气,脱脂棉燃烧,说明CO2、H2O与Na2O2的反应是放热反应 | |
| C. | 滴有酚酞的NaHCO3溶液呈浅红色,微热后红色加深,是因为NaHCO3分解生成了Na2CO3. | |
| D. | 钠长期暴露在空气中的产物是Na2CO3,原因是钠与氧气生成的Na2O与水和二氧化碳反应 |
6.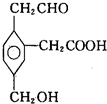 某有机物的结构简式如图所示,在一定条件下对于下列反应:
某有机物的结构简式如图所示,在一定条件下对于下列反应:
①加成、②水解、③酯化、④氧化、⑤中和、⑥消去,其中该物质可能发生的是( )
 某有机物的结构简式如图所示,在一定条件下对于下列反应:
某有机物的结构简式如图所示,在一定条件下对于下列反应:①加成、②水解、③酯化、④氧化、⑤中和、⑥消去,其中该物质可能发生的是( )
| A. | ②③④ | B. | ①③④⑤ | C. | ①③⑤⑥ | D. | ②③④⑤⑥ |
 .
.


 .
.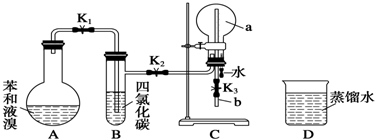
 ,能证明凯库勒观点错误的实验现象是C中产生“喷泉”现象.
,能证明凯库勒观点错误的实验现象是C中产生“喷泉”现象.