题目内容
15.工业上回收利用某合金废料(主要含Fe、Cu、Co、Li等,已知Co、Fe均为中等活泼金属)的工艺流程如图: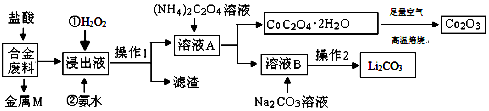
回答下列问题:
( l ) ( NH4)2C2O4中C的化合价为+3.
(2)合金废料加入盐酸浸取,该盐酸不能换为硝酸,原因是硝酸溶解金属时会生成有毒气体,且Cu也溶解在硝酸中,残渣M 的主要成分是一种金属单质,该金属为Cu.
(3)“浸出液”中先后加入的两种试剂涉及氨水、H2O2溶液,应先加入H2O2溶液,加入氨水发生反应的离子方程式为Fe3++3NH3•H2O=Fe(OH)3↓+3NH4+.
(4)溶液A中的金属阳离子是Co2+、Li+,加入(NH4)2C2O4溶液的目的是使Co2+转化为草酸钴沉淀.
(5)“操作l”的名称是过滤.草酸钴高温焙烧生成Co2O3,实验室中高温焙烧使用的仪器是d(填字母).
a.蒸发皿 b.表面皿 c.烧杯 d.坩埚
(6)已知Li2CO3微溶于水,其饱和溶液的浓度与温度关系如表.“操作2”中,蒸发浓缩后需趁热过滤,其目的是减少Li2CO3的溶解损失,90℃时Ksp(Li2CO3)的值为4.0×10-3.
| 温度/℃ | 10 | 30 | 60 | 90 |
| 浓度/mol/L | 0.21 | 0.17 | 0.14 | 0.10 |
分析 合金废料(主要含Fe、Cu、Co、Li等,已知Co、Fe都是中等活泼金属)加入盐酸过滤得到金属M为不与盐酸反应的铜,浸出液中加入过氧化氢氧化亚铁离子为铁离子,加入氨水调节溶液PH使铁离子转化为氢氧化铁沉淀,通过操作Ⅰ过滤得到溶液A中加入草酸铵溶液沉淀钴离子过滤得到溶液B主要是锂离子的溶液,加入碳酸钠沉淀锂离子,过滤得到碳酸锂;结晶析出CoC2O4•2H2O在足量空气中煅烧得到氧化钴,以此解答该题.
解答 解:(1)根据化合价代数和为0,( NH4)2C2O4中C的化合价为+3,故答案为:+3;
(2)因为硝酸溶解金属时会生成有毒气体,且Cu也溶解在硝酸中,所以盐酸不能换为硝酸,上述分析判断金属M为Cu,故答案为:硝酸溶解金属时会生成有毒气体,且Cu也溶解在硝酸中;Cu;
(3)加入H2O2的作用是氧化亚铁离子为铁离子,加入氨水的作用是调节溶液PH使Fe3+转化为Fe(OH)3沉淀,离子方程式为:Fe3++3NH3•H2O=Fe(OH)3↓+3NH4+,所以应先加入H2O2溶液,
故答案为:H2O2溶液;Fe3++3NH3•H2O=Fe(OH)3↓+3NH4+;
(4)根据以上分析,溶液A中的金属阳离子是Co2+、Li+,加入(NH4)2C2O4溶液的目的是使Co2+转化为草酸钴沉淀,故答案为:Co2+、Li+;使Co2+转化为草酸钴沉淀;
(5)根据以上分析,“操作l”的名称是过滤,草酸钴高温焙烧生成Co2O3,实验室中高温焙烧使用的仪器是坩埚,
故答案为:过滤;d;
(6)Li2CO3微溶于水,溶解度随温度升高而降低,为减少Li2CO3的溶解损失,蒸发浓缩后必须趁热过滤,90℃时c(Li2CO3)的浓度为0.10mol/L,则c(Li+)=0.20mol/L,c(CO32-)=0.10mol/L,则Ksp(Li2CO3)=0.20×0.20×0.10=4.0×10-3,
故答案为:减少Li2CO3的溶解损失;4.0×10-3.
点评 本题主要考查物质的分离提纯的综合应用,为高频考点,侧重于学生的分析能力和实验能力、计算能力的考查,综合性强,注意把握实验的流程和原理,难度中等.

 阅读快车系列答案
阅读快车系列答案| A. | 钠的熔点低 | B. | 钠的密度小 | C. | 钠的硬度小 | D. | 有强还原性 |
| A. | 电池放电时正极上有气泡产生 | B. | 电池放电时Cl-由负极向正极迁移 | ||
| C. | 正极反应式为Ag++e-=Ag | D. | 负极副反应为Mg+H2O=Mg(OH)2+H2↑ |
| A. | 镀锡铁制品镀层破损后铁不易被腐蚀 | |
| B. | 相同温度下,pH相同的盐酸和硫酸中水的电离程度相同 | |
| C. | 向饱和石灰水中滴加少量CuC12溶液出现蓝色沉淀,则Ksp[Ca(OH)2]<Ksp[Cu(OH)2] | |
| D. | 合成氨生产中,需将NH3液化分离,目的是加快正反应速率,并提高H2转化率 |

| A. | “吹出”采用热空气而不是常温空气的原因是热空气氧化性强 | |
| B. | 碱液吸收所发生的化学反应中氧化剂与还原剂之比为1:5 | |
| C. | 第③步中“酸化”要用强氧化性的酸,如硝酸 | |
| D. | 含溴的水溶液B中的单质溴浓度比A中的大 |
| A. | 原素Z、W的简单离子的电子层结构不同 | |
| B. | Y的最高价氧化物的水化物能与其简单气态氢化物反应生成盐且显碱性 | |
| C. | 由X元素形成的单质不一定是原子晶体 | |
| D. | 由X、Y、Z、M四种元素形成的化合物一定既有离子键,又有共价键 |
| 选项 | 实验操作 | 现象 | 结论 |
| A | 将KI和H2O2溶液在试管中混合后,加入苯萃取,振荡,静置 | 上层溶液呈紫红色 | 氧化性:H2O2>I2 |
| B | 将刚刚用砂纸打磨过的铝箔放在酒精灯上加热 | 铝箔熔化,但不滴落 | 铝易被氧化;铝的熔点比氧化铝低 |
| C | 常温下,用pH试纸测量某浓度的NaHSO3溶液的pH | pH约为5.5 | 该溶液中的HSO3-的电离程度大于它的水解程度 |
| D | 向盛Mg(OH)2悬浊液的试管中加入适量NH4Cl浓溶液 | 溶液变澄清 | Mg(OH)2与NH4Cl溶液发生氧化还原反应 |
| A. | A | B. | B | C. | C | D. | D |
| 化学键 | C-C | C-H | H-H | C-O | C≡O | H-O |
| 键能 (kJ•mol-1) | 348 | 413 | 436 | 358 | 1072 | 463 |
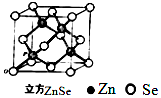 硒化锌是一种透明色半导体,也可作为红光外学材料,熔点1520℃.
硒化锌是一种透明色半导体,也可作为红光外学材料,熔点1520℃.