题目内容
下列反应的离子方程式书写正确的是( )
| A、NaHSO3在水中的电离:NaHSO3═Na++H++SO32- |
| B、碳酸钠水溶液的水解:CO32-+2H2O?H2CO3+2OH- |
| C、向含有Pb2+的工业废水中加入FeS:Pb2++FeS═PbS↓+Fe2+ |
| D、向硫酸铜溶液中滴加过量氨水:Cu2++2NH3?H2O═Cu(OH)2↓+2NH4+ |
考点:离子方程式的书写
专题:离子反应专题
分析:A.亚硫酸氢根离子为弱酸的酸式根离子应保留化学式;
B.碳酸根离子为弱酸的酸式根离子分步水解;
C.硫化铅的溶解度小于硫化亚铁;
D.向硫酸铜溶液中滴加过量氨水生成可溶性络合物.
B.碳酸根离子为弱酸的酸式根离子分步水解;
C.硫化铅的溶解度小于硫化亚铁;
D.向硫酸铜溶液中滴加过量氨水生成可溶性络合物.
解答:
解:A.NaHSO3在水中的电离,离子方程式:NaHSO3═Na++HSO3-,故A错误;
B.碳酸钠水溶液的水解,离子方程式:CO32-+H2O?HCO3-+OH-,故B错误;
C.硫化铅的溶解度小于硫化亚铁,向含有Pb2+的工业废水中加入FeS反应生成硫化铅沉淀,离子方程式为:Pb2++FeS═PbS↓+Fe2+,故C正确;
D.向硫酸铜溶液中滴加过量氨水,离子方程式:Cu2++4NH3?H2O=[Cu(NH3)4]2++4H2O,故D错误;
故选:C.
B.碳酸钠水溶液的水解,离子方程式:CO32-+H2O?HCO3-+OH-,故B错误;
C.硫化铅的溶解度小于硫化亚铁,向含有Pb2+的工业废水中加入FeS反应生成硫化铅沉淀,离子方程式为:Pb2++FeS═PbS↓+Fe2+,故C正确;
D.向硫酸铜溶液中滴加过量氨水,离子方程式:Cu2++4NH3?H2O=[Cu(NH3)4]2++4H2O,故D错误;
故选:C.
点评:本题考查了离子方程式的书写,明确反应的实质是解题关键,注意化学式的拆分、电解质的强弱,题目难度不大.

练习册系列答案
 一诺书业暑假作业快乐假期云南美术出版社系列答案
一诺书业暑假作业快乐假期云南美术出版社系列答案
相关题目
下列叙述正确的是( )
| A、放热反应在任何温度下均能自发进行 |
| B、自发过程指的是常温下,不借助外力就能自动进行的过程 |
| C、熵增加的放热反应在任何温度下均能自发进行 |
| D、对于同一物质,其熵值大小为S(g)<S(l)<S(s) |
下列化学用语正确的是( )
A、
 | ||
B、某有机物的分子的简易球棍模型如图,分子式为C3H7O2N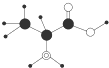 | ||
C、羟基乙酸(HOCH2COOH)的缩聚物: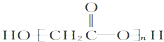 | ||
| D、铁在元素周期表中位于第4周期第ⅧB 族 |
NA表示阿伏伽德罗常数,下列说法正确的是( )
| A、1molNa2O2与任何物质反应时转移的电子数都是1NA |
| B、1L 2mol?L-1MgCl2溶液中含有的Cl-数为2NA |
| C、标准状况下,11.2L氯气与足量稀NaOH溶液反应转移电子数为0.5NA |
| D、标准状况下,2.24L CO2与2.24L H2O中所含原子数均为0.3NA |
下列表示碳酸氢钠水解的离子方程式正确的是( )
| A、HCO3-+H+═CO2↑+H2O |
| B、HCO3-+OHˉ═CO32-+H2O |
| C、HCO3-+H2O═H3O++CO32- |
| D、HCO3-+H2O?H2CO3+OH- |
0.5L AlCl3溶液中含有Cl-9.03×1023个,则该AlCl3溶液的物质的量浓度为( )
| A、0.1mol?L-1 |
| B、1mol?L-1 |
| C、3mol?L-1 |
| D、1.5mol?L-1 |
下列物质按纯净物、混合物、电解质、非电解质的组合正确的是( )
| 纯净物 | 混合物 | 强电解质 | 弱电解质 | 非电解质 | |
| A | 盐酸 | 水煤气 | 硫酸 | 醋酸 | H2 |
| B | 胆矾 | 石灰水 | 硫酸钡 | H2CO3 | NH3 |
| C | 火碱 | 蔗糖溶液 | 氯化钠 | 氨水 | 三氧化硫 |
| D | 干冰 | 波尔多液 | 苛性钾 | 氯化氢 | 乙醇 |
| A、A | B、B | C、C | D、D |
当用标准盐酸溶液滴定待测氢氧化钠溶液时,下列操作中会使测定结果偏低的是( )
| A、用酸式滴定管滴至终点时,俯视滴定管读数 |
| B、将碱液移入锥形瓶后,加了10 ml蒸馏水再滴定 |
| C、酸式滴定管用蒸馏水润洗后,未用标准盐酸溶液润洗 |
| D、酸式滴定管注入酸液时,尖嘴处留有气泡,达滴定终点时气泡消失 |

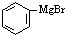 、
、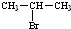 为主要原料制备
为主要原料制备 的合成路线流程图(无机试剂任用)
的合成路线流程图(无机试剂任用)