题目内容
NA表示阿伏伽德罗常数,下列说法正确的是( )
| A、1molNa2O2与任何物质反应时转移的电子数都是1NA |
| B、1L 2mol?L-1MgCl2溶液中含有的Cl-数为2NA |
| C、标准状况下,11.2L氯气与足量稀NaOH溶液反应转移电子数为0.5NA |
| D、标准状况下,2.24L CO2与2.24L H2O中所含原子数均为0.3NA |
考点:阿伏加德罗常数
专题:阿伏加德罗常数和阿伏加德罗定律
分析:A、根据过氧化钠中的氧元素为-1价及发生氧化还原反应的类型判断.
B、求出氯化镁的物质的量,然后根据1mol氯化镁含2mol氯离子来分析;
C、氯气的物质的量为0.5mol,氯气与氢氧化钠溶液的反应中,氯气既是氧化剂也是还原剂;
D、标况下,水为液态.
B、求出氯化镁的物质的量,然后根据1mol氯化镁含2mol氯离子来分析;
C、氯气的物质的量为0.5mol,氯气与氢氧化钠溶液的反应中,氯气既是氧化剂也是还原剂;
D、标况下,水为液态.
解答:
解:A、1mol Na2O2参加氧化还原反应时,若完全作氧化剂,转移的电子数为2mol;若发生自身的氧化还原反应,转移的电子的物质的量为1mol,所以转移的电子数不一定为NA,故A错误;
B、氯化镁的物质的量n=CV=1L×1mol/L=1mol,而1mol氯化镁含2mol氯离子,故2mol氯化镁含有4mol氯离子,故B错误;
C、Cl2的物质的量为0.5mol,1mol氯气与足量的NaOH溶液反应转移了1mol电子,故0.5mol氯气转移的电子数为0.5NA,故C正确;
D、标况下,水为液态,故D错误.
故选C.
B、氯化镁的物质的量n=CV=1L×1mol/L=1mol,而1mol氯化镁含2mol氯离子,故2mol氯化镁含有4mol氯离子,故B错误;
C、Cl2的物质的量为0.5mol,1mol氯气与足量的NaOH溶液反应转移了1mol电子,故0.5mol氯气转移的电子数为0.5NA,故C正确;
D、标况下,水为液态,故D错误.
故选C.
点评:本题考查了阿伏伽德罗常数的有关计算,熟练掌握公式的使用和物质的结构是解题关键,难度不大.

练习册系列答案
相关题目
反应3A+B=2C+D在四种不同情况下的反应速率分别为:
①v(A)=0.15mol/(L?s);②v(B)=0.06mol/(L?s);③v(C)=0.05mol/(L?s);④v(D)=0.045mol/(L?s).则反应进行由快到慢的顺序为( )
①v(A)=0.15mol/(L?s);②v(B)=0.06mol/(L?s);③v(C)=0.05mol/(L?s);④v(D)=0.045mol/(L?s).则反应进行由快到慢的顺序为( )
| A、④>③>①>② |
| B、②>④>③>① |
| C、②>①>④>③ |
| D、④>③>②>① |
已知3375As、3579Br位于同一周期.下列关系正确的是( )
| A、原子半径:As>Cl>P |
| B、热稳定性:HCl>AsH3>HBr |
| C、还原性:As3->S2->Cl- |
| D、酸性:H3AsO4>H2SO4>H3PO4 |
NA表示阿伏加德罗常数,下列说法正确的是( )
| A、标准状况下,22.4L的CCl4中含有的CCl4分子数为NA |
| B、10mL pH=6的纯水中含有OH-离子数为10-10 NA |
| C、100 mL 1 mol?L-1 的Na2CO3溶液中含有CO32-离子数为0.1NA |
| D、14g由N2与CO组成的混合气体含有的原子数目为NA |
某离子反应涉及H2O、ClO-、I03-、OH-、I2、Cl-六种微粒.其中c(ClO-)随反应进行逐渐减小.下列判断错误的是( )
| A、该反应的还原剂是I2 |
| B、氧化剂与还原剂的物质的量之比为5:2 |
| C、消耗lmol氧化剂,转移2mol电子 |
| D、反应后溶液的碱性明显减弱 |
以下是几种常用基本物理量的名称与符号的对应关系,其中不正确的是( )
| A、物质的量--mol |
| B、质量--m |
| C、时间--t |
| D、电流--I |
下列反应的离子方程式书写正确的是( )
| A、NaHSO3在水中的电离:NaHSO3═Na++H++SO32- |
| B、碳酸钠水溶液的水解:CO32-+2H2O?H2CO3+2OH- |
| C、向含有Pb2+的工业废水中加入FeS:Pb2++FeS═PbS↓+Fe2+ |
| D、向硫酸铜溶液中滴加过量氨水:Cu2++2NH3?H2O═Cu(OH)2↓+2NH4+ |
无土栽培中,需配制一种含 50mol NH4Cl、16mol KCl 和24mol K2SO4的营养液.若用 KCl、NH4Cl 和 (NH4)2SO4 三种固体为原料来配制,其物质的量分别为( )
| A、2 mol、64 mol、24 mol |
| B、64 mol、2 mol、24 mol |
| C、32 mol、50 mol、12 mol |
| D、16 mol、50 mol、24 mol |
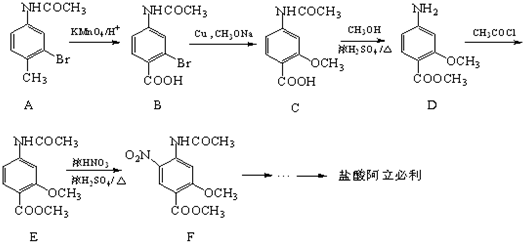
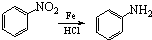 .请写出以
.请写出以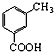 、CH3CH2CH2COCl、CH3OH为原料制备
、CH3CH2CH2COCl、CH3OH为原料制备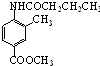 的合成路线流程图(无机试剂任用).合成路线流程图示例如图:
的合成路线流程图(无机试剂任用).合成路线流程图示例如图: .
.