题目内容
以KCl和ZnCl2混合液为电镀液在铁制品上镀锌,下列说法正确的是( )
| A、未通电前上述镀锌装置可构成原电池,电镀过程是该原电池的充电过程 |
| B、因部分电能转化为热能,电镀时通过的电量与锌的析出量无确定关系 |
| C、铁制品应该连接在直流电源的负极 |
| D、镀锌层破损后即对铁制品失去保护作用 |
考点:电解原理
专题:电化学专题
分析:A、根据Zn的金属性强于Fe,未通电前上述镀锌装置可构成原电池,其正极反应为:O2+4e-+2H2O═4OH-,与电镀时所发生的反应为不同的两个反应,故电镀过程不是该原电池的充电过程;
B、电镀时,每转移2mol电子析出1molZn,通过的电量与析出的锌的量存在确定的关系,与能量的其他转化无关;
C、电镀时,镀件是阴极,镀层金属是阳极,电镀液是含有镀层金属阳离子的盐溶液;
D、镀锌铁制品的镀层破损后,易形成Zn-Fe原电池,Zn作负极优先被腐蚀,铁制品仍能受到保护.
B、电镀时,每转移2mol电子析出1molZn,通过的电量与析出的锌的量存在确定的关系,与能量的其他转化无关;
C、电镀时,镀件是阴极,镀层金属是阳极,电镀液是含有镀层金属阳离子的盐溶液;
D、镀锌铁制品的镀层破损后,易形成Zn-Fe原电池,Zn作负极优先被腐蚀,铁制品仍能受到保护.
解答:
解:A、未通电前上述镀锌装置可构成原电池,因原电池反应与电镀时所发生的反应为不同的两个反应,故电镀过程不是该原电池的充电过程,故A错误;
B、电解过程中确实存在电能转化成热能的情况,但电镀时通过的电量与析出的锌的量存在确定的关系,与能量的其他转化无关,故B错误;
C、在铁制品上镀锌,镀件铁制品应该做阴极,连接在直流电源的负极上,故C正确;
D、镀锌层破损后,能形成锌铁原电池,铁为正极,锌为负极,同样起到保护铁的作用,故D错误.
故选C.
B、电解过程中确实存在电能转化成热能的情况,但电镀时通过的电量与析出的锌的量存在确定的关系,与能量的其他转化无关,故B错误;
C、在铁制品上镀锌,镀件铁制品应该做阴极,连接在直流电源的负极上,故C正确;
D、镀锌层破损后,能形成锌铁原电池,铁为正极,锌为负极,同样起到保护铁的作用,故D错误.
故选C.
点评:此题考查了原电池与电解池的工作原理及应用.重在突出应用及电路中的电量与析出物质的守恒关系,解答本题时应明确电池或电解工作原理,对于其应用也要掌握.

练习册系列答案
相关题目
下列表述正确的是( )
A、H2O2的电子式: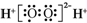 | ||
B、Cl的原子结构示意图: | ||
C、质子数是82,中子数是122的铅原子:
| ||
D、CO2的比例模型: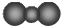 |
现有MgCl2、AlCl3、CuCl2、FeCl3、NH4Cl五种溶液,只用一种试剂把它们区别开来,这种试剂是( )
| A、氨水 |
| B、AgNO3 |
| C、NaOH |
| D、H2SO4 |

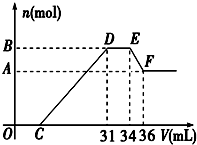 已知硝酸与金属发生氧化还原反应的时候,一般硝酸浓度越稀,对应的还原产物中氮的化合价越低.现有一定量的铝、铁合金与一定量稀HNO3充分反应,反应过程中无任何气体放出.在反应结束后的溶液中,逐滴加入4mol/L NaOH溶液,所加NaOH溶液的体积(V)与产生沉淀的物质的量(n)关系如图所示.则:
已知硝酸与金属发生氧化还原反应的时候,一般硝酸浓度越稀,对应的还原产物中氮的化合价越低.现有一定量的铝、铁合金与一定量稀HNO3充分反应,反应过程中无任何气体放出.在反应结束后的溶液中,逐滴加入4mol/L NaOH溶液,所加NaOH溶液的体积(V)与产生沉淀的物质的量(n)关系如图所示.则: