题目内容
20.有以下9种物质:①Ne;②NH4Cl;③KNO3;④NaOH;⑤Cl2;⑥SO2;⑦H2S;⑧Na2O2;⑨MgCl2.请用上述物质的数字序号填空:
(1)只存在离子键的是⑨.
(2)只存在共价键的是⑤⑥⑦.
(3)只存在共价键的电解质是⑦.
(4)既存在离子键又存在共价键的是②③④⑧.
(5)不存在化学键的是①.
分析 活泼金属和活泼非金属元素之间易形成离子键,非金属元素之间易形成共价键,只含共价键的化合物是共价化合物,含有离子键的化合物是离子化合物,离子化合物中可能含有共价键,在水溶液中或熔融状态下能导电的化合物是电解质,据此分析解答.
解答 解:①Ne为单原子分子,不存在化学键,只存在分子间作用力;
②NH4Cl ③KNO3、④NaOH、⑧Na2O2中含有离子键和共价键,为离子化合物;
⑤Cl2中只含共价键,为单质;
⑥SO2⑦H2S中只含共价键,为共价化合物,但硫化氢是电解质;
⑨MgCl2中只含离子键,为离子化合物;
(1)只存在离子键的是⑨,故答案为:⑨;
(2)只存在共价键的是⑤⑥⑦,故答案为:⑤⑥⑦;
(3)只存在共价键的电解质是⑦,故答案为:⑦;
(4)既存在离子键又存在共价键的是②③④⑧,故答案为:②③④⑧;
(5)不存在化学键的是①,故答案为:①.
点评 本题考查化学键和化合物的判断,侧重考查基本概念,明确物质构成微粒及微粒之间作用力是解本题关键,题目难度不大.

练习册系列答案
相关题目
13.MnO2和锌是制造干电池的主要原料.
电解法生产MnO2传统的工艺主要流程为:软锰矿加煤还原焙烧;用硫酸浸出焙烧料;浸出液(主要含Mn2+)经净化后再进行电解.
90年代后期发明了生产MnO2和锌的新工艺,主要是采用软锰矿(主要成分为MnO2,含少量Al2O3和SiO2杂质)和闪锌矿(主要成分为ZnS,含少量FeS、CuS、CdS杂质)为主要原料,经过除杂后,得到含Zn2+、Mn2+离子的溶液,再通过电解同时获得MnO2和锌.简化流程框图如下(中间产物的固体部分已经略去):
 已知各种金属离子完全沉淀的pH如下表:
已知各种金属离子完全沉淀的pH如下表:
回答下列问题:
(1)步骤①中,软锰矿、闪锌矿粉与硫酸溶液共热时析出硫的反应为氧化还原反应,例如:MnO2+ZnS+2H2SO4=MnSO4+ZnSO4+S↓+2H2O,请写出MnO2在酸性溶液中分别和CuS和FeS发生反应的化学方程式:MnO2+CuS+2H2SO4=MnSO4+CuSO4+S↓+2H2O、MnO2+2FeS+6H2SO4=Fe2(SO4)3+3MnSO4+2S↓+6H2O.
(2)步骤②加入金属锌是为了回收金属,回收金属的主要成份为Cu、Cd(用化学符号表示)
(3)步骤③物质C由多种物质组成,其中含有两种固体,其中一种为MnO2,其作用是将Fe2+氧化为Fe3+
此空删去,另外一种固体物质可为Zn(OH)2.
(4)步骤④中电解过程中MnO2在阳极析出,该电极上发生的反应方程式为Mn2+-2e-+2H2O=MnO2+4H+.产品D的化学式为H2SO4,该物质对整个生产的意义是用于溶解软锰矿和闪锌矿,循环使用.
电解法生产MnO2传统的工艺主要流程为:软锰矿加煤还原焙烧;用硫酸浸出焙烧料;浸出液(主要含Mn2+)经净化后再进行电解.
90年代后期发明了生产MnO2和锌的新工艺,主要是采用软锰矿(主要成分为MnO2,含少量Al2O3和SiO2杂质)和闪锌矿(主要成分为ZnS,含少量FeS、CuS、CdS杂质)为主要原料,经过除杂后,得到含Zn2+、Mn2+离子的溶液,再通过电解同时获得MnO2和锌.简化流程框图如下(中间产物的固体部分已经略去):
 已知各种金属离子完全沉淀的pH如下表:
已知各种金属离子完全沉淀的pH如下表:| Zn2+ | Mn2+ | Fe2+ | Fe3+ | Al3+ | |
| pH | 8.0 | 10.1 | 9.0 | 3.2 | 4.7 |
(1)步骤①中,软锰矿、闪锌矿粉与硫酸溶液共热时析出硫的反应为氧化还原反应,例如:MnO2+ZnS+2H2SO4=MnSO4+ZnSO4+S↓+2H2O,请写出MnO2在酸性溶液中分别和CuS和FeS发生反应的化学方程式:MnO2+CuS+2H2SO4=MnSO4+CuSO4+S↓+2H2O、MnO2+2FeS+6H2SO4=Fe2(SO4)3+3MnSO4+2S↓+6H2O.
(2)步骤②加入金属锌是为了回收金属,回收金属的主要成份为Cu、Cd(用化学符号表示)
(3)步骤③物质C由多种物质组成,其中含有两种固体,其中一种为MnO2,其作用是将Fe2+氧化为Fe3+
此空删去,另外一种固体物质可为Zn(OH)2.
(4)步骤④中电解过程中MnO2在阳极析出,该电极上发生的反应方程式为Mn2+-2e-+2H2O=MnO2+4H+.产品D的化学式为H2SO4,该物质对整个生产的意义是用于溶解软锰矿和闪锌矿,循环使用.
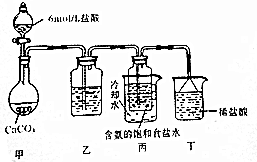
11.浓氨水可与新制生石灰作用生成氨气,干燥的氨气在高温下能被CuO氧化成N2实验室欲用图仪器装置和药品来制取纯净的氮气.
试回答下列问题:
(1)这些装置按气流方向自左向右的连接顺序是(填A、B、C…)F→G→H→A→B→D→C(A、B顺序可颠倒).
(2)E中发生反应的化学方程式是CaO+NH3•H2O=Ca(OH)2+NH3↑.
(3)装置④中应当选用的干燥剂是(写名称)碱石灰.
(4)装置①中发生氧化还原反应的化学方程式是2NH3+3CuO$\frac{\underline{\;\;△\;\;}}{\;}$N2↑3H2O+3Cu.其中氧化剂是CuO,氧化产物是N2(写化学式).
(5)装置②中浓硫酸的作用是除去水蒸气和氨气.
| 序号 | ① | ② | ③ | ④ |
| 仪器装置 | 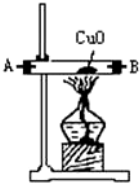 | 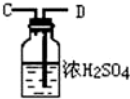 | 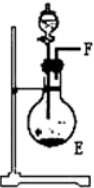 |  |
(1)这些装置按气流方向自左向右的连接顺序是(填A、B、C…)F→G→H→A→B→D→C(A、B顺序可颠倒).
(2)E中发生反应的化学方程式是CaO+NH3•H2O=Ca(OH)2+NH3↑.
(3)装置④中应当选用的干燥剂是(写名称)碱石灰.
(4)装置①中发生氧化还原反应的化学方程式是2NH3+3CuO$\frac{\underline{\;\;△\;\;}}{\;}$N2↑3H2O+3Cu.其中氧化剂是CuO,氧化产物是N2(写化学式).
(5)装置②中浓硫酸的作用是除去水蒸气和氨气.
12.下列根据实验事实得出的结论错误的是( )
| 实验事实 | 结论 | |
| A | 加碱加热产生使湿润红色石蕊试纸变蓝的气体 | 溶液中含有NH4+ |
| B | 加BaCl2溶液有白色沉淀,加稀硝酸沉淀不溶解 | 该溶液中一定含有SO42- |
| C | 加KSCN溶液无现象•再滴加氯水变血红 | 溶液中有Fe2+ |
| D | 加热时.铜能与浓硫酸反应 | 浓硫酸有强氧化性 |
| A. | A | B. | B | C. | C | D. | D |
10.常温下,有体积相同的四种溶液:①pH=2的CH3COOH溶液;②pH=2的硫酸;③pH=12的氨水;④pH=12的NaOH溶液.下列说法正确的是( )
| A. | ①和②混合后c(H+)=c(CH3COO-)+c(OH-)+2c(SO42-) | |
| B. | ①和④溶液中:c(Na+)=c(CH3COO-)+c(CH3COOH)=0.01mol•L-1 | |
| C. | ②和③混合溶液中:c(SO42-)>c(NH4+)>c(OH-)>c(H+) | |
| D. | 四种溶液各稀释100倍,溶液pH:④>③>①>② |
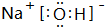 ,CB2的电子式为
,CB2的电子式为 .
.