题目内容
20.标出下列反应中电子转移的方向和数目并回答问题:3H2O2+2H2CrO4→2Cr(OH)3+3O2+2H2O
(1)该反应中的还原剂是H2O2,被还原的元素H2CrO4中的Cr或+6价的Cr,还原产物是O2;
(2)该反应中,发生氧化反应的过程是H2O2→O2;
(3)反应转移了0.3mol电子,则产生的气体在标准状态下体积约为3.36L.
分析 反应3H2O2+2H2CrO4=2Cr(OH)3+3O2+2H2O中,H2CrO4中Cr化合价从+6→+3,得电子,H2O2中0化合价从-1→0,失电子,结合元素化合价解答该题.
解答 解:Cr化合价从+6→+3,得电子,0化合价从-1→0,失电子,因此箭头指向由O指向Cr,电子总数为:2×(6-3)=6,用单线桥法表示反应中电子转移的方向和数目如下: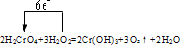 ,
,
(1)该反应中失电子化合价升高的反应物是H2O2,氧化产物是O2,得电子化合价降低的元素是H2CrO4中的Cr或+6价的Cr,所以被还原的元素是Cr6+,则H2CrO4是氧化剂发生还原反应,还原产物是Cr(OH)3,
故答案为:H2O2;H2CrO4中的Cr或+6价的Cr;O2;
(2)该反应中,还原剂发生氧化反应,所以氧化过程为:H2O2→O2,故答案为:H2O2;O2;
(3)根据得失电子守恒得生成氧气的物质的量为$\frac{0.3mol}{2}$═0.15mol,标况下氧气的体积为:0.15mol×22.4L/mol=3.36L,故产生的氧气体积为3.36L,
故答案为:3.36L.
点评 本题考查了还原剂的判断、氧化还原反应的分析及计算,做此类题目要从化合价入手,从化合价的变化来分析和计算,此题易错点为箭头的指向和数目的多少.

练习册系列答案
相关题目
2.图所示的实验装置图正确且能达到相应实验目的是( )
| A. | 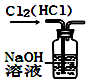 用图所示装置除去Cl2中的HCl | |
| B. | 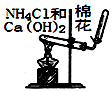 用图所示装置实验室制NH3 | |
| C. | 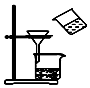 用图所示装置分离MnO2和KCl | |
| D. | 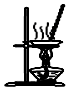 用图所示装置蒸干NH4Cl饱和溶液制备NH4Cl晶体 |
11.下列有关物质的性质和该性质的应用均正确的是( )
| A. | 氯气具有酸性,可与烧碱或石灰乳反应制备含氯消毒剂 | |
| B. | 明矾在水中能形成胶体,可作为净水剂 | |
| C. | 氢氟酸具有弱酸性,可用氢氟酸雕刻玻璃 | |
| D. | 过氧化钠具有强氧化性,可用作潜水艇中氧气的来源 |
8.往100mL0.2mol•L-1的NaOH溶液中通入体积为V(标准状况下)的CO2,充分反应后得到的溶液同时含有Na2CO3和NaHCO3两种溶质.下列关于V的判断,正确的是( )
| A. | <0.224L | B. | 0.224L | C. | 0.224L-0.448L | D. | V>0.448L |
15.上海天原化工厂是我国最早的氯碱企业,其创始人是( )
| A. | 侯德榜 | B. | 吴蕴初 | C. | 荣毅仁 | D. | 钱学森 |
5.下列物质的电子式书写正确的是( )
| A. | Na2O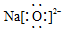 | B. | H2S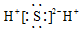 | C. | H2O2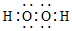 | D. | N2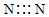 |
12.下列过程吸收热量的是( )
| A. | 水凝结成冰 | B. | 天然气燃烧 | ||
| C. | 盐酸与氢氧化钠中和反应 | D. | 液氨气化 |
9.在实验中,下列说法不正确的是( )
| A. | 制取蒸馏水时,为防止烧瓶内产生暴沸现象,应先向烧瓶中加入几片碎瓷片 | |
| B. | 可以不用任何试剂就可以鉴别AlCl3和NaOH、Na2CO3和HCl、NaAlO2和HCl | |
| C. | 除去CO2气体中混有的少量SO2可以将气体通入KMnO4溶液中或饱和NaHCO3溶液 | |
| D. | H2在Cl2中燃烧火焰呈淡蓝色 |
10.某无色溶液中可能含有Na+、NH4+、Ba2+、Cu2+、SO42-、SO32-、Cl-、Br-、CO32-中的若干种.为检验其中含有的离子,进行如下实验:
①取10mL溶液,加入足量氯水,无气体产生,再加入CCl4溶液分层,下层为橙红色;
②分液后,将①中上层溶液加入足量BaCl2和HCl溶液,产生白色沉淀2.33g;
③另取10mL原溶液,加入过量的浓氢氧化钠溶液并加热,收集到标准状况下448mL气体.
下列关于原溶液的说法正确的是( )
①取10mL溶液,加入足量氯水,无气体产生,再加入CCl4溶液分层,下层为橙红色;
②分液后,将①中上层溶液加入足量BaCl2和HCl溶液,产生白色沉淀2.33g;
③另取10mL原溶液,加入过量的浓氢氧化钠溶液并加热,收集到标准状况下448mL气体.
下列关于原溶液的说法正确的是( )
| A. | 肯定存在NH4+、Cl-、Br- | |
| B. | 是否存在Na+需要通过焰色反应来确定 | |
| C. | SO42-、SO32-至少含有一种 | |
| D. | 肯定不存在Ba2+、Cu2+、SO32-、CO32- |