题目内容
9.在实验中,下列说法不正确的是( )| A. | 制取蒸馏水时,为防止烧瓶内产生暴沸现象,应先向烧瓶中加入几片碎瓷片 | |
| B. | 可以不用任何试剂就可以鉴别AlCl3和NaOH、Na2CO3和HCl、NaAlO2和HCl | |
| C. | 除去CO2气体中混有的少量SO2可以将气体通入KMnO4溶液中或饱和NaHCO3溶液 | |
| D. | H2在Cl2中燃烧火焰呈淡蓝色 |
分析 A.加热液体,防止剧烈沸腾;
B.AlCl3和NaOH、Na2CO3和HCl、NaAlO2和HCl均为与量有关的反应;
C.SO2与KMnO4溶液中或饱和NaHCO3溶液反应,而二氧化碳不能;
D.反应生成HCl,有苍白色火焰.
解答 解:A.制取蒸馏水时,向烧瓶中加入几片碎瓷片,可防止烧瓶内产生暴沸现象,故A正确;
B.AlCl3和NaOH、Na2CO3和HCl、NaAlO2和HCl均为与量有关的反应,量不同,现象不同,则不用任何试剂就可以鉴别,故B正确;
C.SO2与KMnO4溶液中或饱和NaHCO3溶液反应,而二氧化碳不能,则均可除杂,故C正确;
D.H2在Cl2中燃烧,有苍白色火焰,故D错误;
故选D.
点评 本题考查化学实验方案的评价,为高频考点,把握物质的性质、混合物分离提纯实验、物质鉴别、实验技能为解本题关键,侧重分析与实验能力的考查,注意实验的评价性分析,题目难度不大.

练习册系列答案
相关题目
19.2015年9月3日抗战胜利70周年大阅兵场上,展示了我国研制的各种导弹,导弹之所以有神奇的命中率,是制造导弹合金材料中的稀土元素钕(60140Nd)的贡献.则下列说法中正确的是( )
| A. | 钕原子的摩尔质量等于其相对原子质量 | |
| B. | 一个${\;}_{60}^{140}Nd$原子的质量为$\frac{140}{{N}_{A}}$g | |
| C. | ${\;}_{60}^{140}Nd$原子的中子数与质子数之差为80 | |
| D. | 14g钕中含10mol电子 |
17.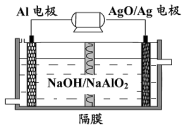 铝电池性能优越,Al-AgO电池可用作水下动力电源,其原理如图所示.电池反应为:2Al+3AgO+2NaOH=2NaAlO2+3Ag+H2O下列说法中错误的是( )
铝电池性能优越,Al-AgO电池可用作水下动力电源,其原理如图所示.电池反应为:2Al+3AgO+2NaOH=2NaAlO2+3Ag+H2O下列说法中错误的是( )
 铝电池性能优越,Al-AgO电池可用作水下动力电源,其原理如图所示.电池反应为:2Al+3AgO+2NaOH=2NaAlO2+3Ag+H2O下列说法中错误的是( )
铝电池性能优越,Al-AgO电池可用作水下动力电源,其原理如图所示.电池反应为:2Al+3AgO+2NaOH=2NaAlO2+3Ag+H2O下列说法中错误的是( )| A. | 该装置可实现化学能向电能的转化 | B. | 电池工作时AgO得到电子 | ||
| C. | Al是负极 | D. | OH-透过隔膜向AgO/Ag极迁移 |
4.下列实验设计,不能达到实验目的是( )
| A. | 用CCl4将溴从溴水中提取出来 | |
| B. | 用丁达尔效应鉴别淀粉胶体和食盐溶液 | |
| C. | 采用加热的方法除去碳酸钠固体中混有的碳酸氢钠 | |
| D. | 向某无色溶液中加入硝酸银产生白色沉淀,证明溶液中含有Cl- |
14.某CuSO4、Fe2(SO4)3、H2SO4的混合溶液100mL,SO42-的物质的量浓度为9mol/L,加入足量铁粉,则反应后的溶液中Fe2+离子浓度为(假设反应前后溶液体积不变)( )
| A. | 4.5mol/L | B. | 18mol/L | C. | 3mol/L | D. | 9mol/L |
1.某次硫酸铜晶体结晶水含量的测定实验中,相对误差为-2.7%,原因可能是( )
| A. | 实验时坩埚未完全干燥 | B. | 加热后固体颜色有少量变黑 | ||
| C. | 加热过程中晶体有少量溅失 | D. | 加热后固体未放入干燥器中冷却 |
18.用食用白醋(醋酸浓度约1mol•L-1)进行下列实验,能证明醋酸为弱电解质的是( )
| A. | 向白醋中加入镁粉出现气泡 | B. | 用pH试纸测试其pH约为2 | ||
| C. | 用白醋做导电性实验,灯泡发亮 | D. | 向Cu(OH)2中加入白醋,Cu(OH)2溶解 |
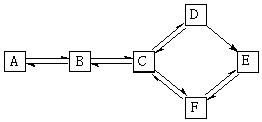 有A、B、C、D、E、F六种有机化合物,存在下图所示转化关系.已知A属于烃,且相对分子质量不超过30;在加热条件下,B可与氢氧化钠溶液反应,向反应后所得液中加入过量的硝酸,再加入硝酸银溶液,生成淡黄色沉淀.
有A、B、C、D、E、F六种有机化合物,存在下图所示转化关系.已知A属于烃,且相对分子质量不超过30;在加热条件下,B可与氢氧化钠溶液反应,向反应后所得液中加入过量的硝酸,再加入硝酸银溶液,生成淡黄色沉淀.