题目内容
8.往100mL0.2mol•L-1的NaOH溶液中通入体积为V(标准状况下)的CO2,充分反应后得到的溶液同时含有Na2CO3和NaHCO3两种溶质.下列关于V的判断,正确的是( )| A. | <0.224L | B. | 0.224L | C. | 0.224L-0.448L | D. | V>0.448L |
分析 国际化n=cV计算出100mL0.2mol•L-1的NaOH溶液中含有氢氧化钠的物质的量,然后根据钠离子守恒利用极值法判断二氧化碳的物质的量,最后根据V=nVm计算出V的范围.
解答 解:100mL0.2mol•L-1的NaOH溶液中含有氢氧化钠的物质的量为:n(NaOH)=0.2mol/L×0.L=0.02mol,
通入CO2充分反应后得到的溶液同时含有Na2CO3和NaHCO3两种溶质,当溶质完全为Na2CO3时,根据质量守恒可知通入二氧化碳的物质的量为:n(CO2)=n(Na2CO3)=$\frac{1}{2}$n(NaOH)=0.01mol,标准状况下0.01mol二氧化碳的体积为:22.4L/mol×0.01mol=0.224L;
当反应后溶质完全为NaHCO3时,则n(CO2)=n(Na2CO3)=n(NaOH)=0.02mol,标准状况下0.01mol二氧化碳的体积为:22.4L/mol×0.02mol=0.448L,
由于反应后溶质为Na2CO3和NaHCO3的混合物,则V的范围为0.224L-0.448L,
故选C.
点评 本题考查了化学方程式的计算,题目难度不大,明确发生反应实质为解答关键,注意掌握讨论法及守恒思想在化学计算后者的应用,试题培养了学生的化学计算能力.

练习册系列答案
相关题目
10.下列能使品红溶液褪色的是( )
| A. | CO2 | B. | Na2SO3 | C. | Cl2 | D. | HCl |
19.2015年9月3日抗战胜利70周年大阅兵场上,展示了我国研制的各种导弹,导弹之所以有神奇的命中率,是制造导弹合金材料中的稀土元素钕(60140Nd)的贡献.则下列说法中正确的是( )
| A. | 钕原子的摩尔质量等于其相对原子质量 | |
| B. | 一个${\;}_{60}^{140}Nd$原子的质量为$\frac{140}{{N}_{A}}$g | |
| C. | ${\;}_{60}^{140}Nd$原子的中子数与质子数之差为80 | |
| D. | 14g钕中含10mol电子 |
16.设NA为阿伏加德罗常数,下列说法正确的是( )
| A. | 一定条件下,6.4 g铜与过量的硫反应,转移电子数目为0.2NA | |
| B. | 3mol单质Fe完全转变为Fe3O4,失去8NA个电子 | |
| C. | 标准状况下,11.2L 水蒸气中含有3NA个原子 | |
| D. | 用石灰乳完全吸收1 mol Cl2时,转移电子的数目是NA |
13.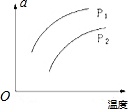 在容积一定的密闭容器中发生可逆反应X(g)+3Y(g)?nZ(g);△H>0,平衡移动关系如图所示.下列说法正确的是( )
在容积一定的密闭容器中发生可逆反应X(g)+3Y(g)?nZ(g);△H>0,平衡移动关系如图所示.下列说法正确的是( )
 在容积一定的密闭容器中发生可逆反应X(g)+3Y(g)?nZ(g);△H>0,平衡移动关系如图所示.下列说法正确的是( )
在容积一定的密闭容器中发生可逆反应X(g)+3Y(g)?nZ(g);△H>0,平衡移动关系如图所示.下列说法正确的是( )| A. | a可能表示混合气体的密度 | |
| B. | 若n=3,p1>p2,则a可表示Y的质量分数 | |
| C. | 若n=3,p1>p2,则a可表示Y的转化率 | |
| D. | a不可能表示混合气体的平均摩尔质量 |
17.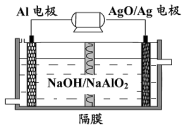 铝电池性能优越,Al-AgO电池可用作水下动力电源,其原理如图所示.电池反应为:2Al+3AgO+2NaOH=2NaAlO2+3Ag+H2O下列说法中错误的是( )
铝电池性能优越,Al-AgO电池可用作水下动力电源,其原理如图所示.电池反应为:2Al+3AgO+2NaOH=2NaAlO2+3Ag+H2O下列说法中错误的是( )
 铝电池性能优越,Al-AgO电池可用作水下动力电源,其原理如图所示.电池反应为:2Al+3AgO+2NaOH=2NaAlO2+3Ag+H2O下列说法中错误的是( )
铝电池性能优越,Al-AgO电池可用作水下动力电源,其原理如图所示.电池反应为:2Al+3AgO+2NaOH=2NaAlO2+3Ag+H2O下列说法中错误的是( )| A. | 该装置可实现化学能向电能的转化 | B. | 电池工作时AgO得到电子 | ||
| C. | Al是负极 | D. | OH-透过隔膜向AgO/Ag极迁移 |
18.用食用白醋(醋酸浓度约1mol•L-1)进行下列实验,能证明醋酸为弱电解质的是( )
| A. | 向白醋中加入镁粉出现气泡 | B. | 用pH试纸测试其pH约为2 | ||
| C. | 用白醋做导电性实验,灯泡发亮 | D. | 向Cu(OH)2中加入白醋,Cu(OH)2溶解 |