题目内容
16.新型储氢材料是开发利用氢能的重要研究方向.(1)Ti(BH4)3是一种储氢材料,可由TiCl4和LiBH4反应制得.
①基态Cl原子中,电子占据的最高能层符号为M,该能层具有的原子轨道数为9.
②LiBH4由Li+和BH4-构成,BH4-的立体结构是正四面体,B原子的杂化轨道类型是sp3.
Li、B、H元素的电负性由大到小排列顺序为H>B>Li.
(2)金属氢化物是具有良好发展前景的储氢材料.
①LiH中,离子半径Li+<H-(填“>”、“=”或“<”).②某储氢材料是第三周期金属元素M的氢化物.M的部分电离能如表所示:
| I1/kJ•mol-1 | I2/kJ•mol-1 | I3/kJ•mol-1 | I4/kJ•mol-1 | I5/kJ•mol-1 |
| 738 | 1451 | 7733 | 10540 | 13630 |
(3)NaH具有NaCl型晶体结构,已知NaH晶体的晶胞参数a=488pm(棱长),Na+半径为102pm,H-的半径为142pm,NaH的理论密度是$\frac{24×4}{{N}_{A}×48{8}^{3}×1{0}^{-30}}$g•cm-3(只列算式,不必计算出数值,阿伏加德罗常数为NA)
分析 (1)①Cl原子核外电子数为17,基态原子核外电子排布为1s22s22p63s23p5,据此解答;
②根据价层电子对互斥理论确定离子空间构型、B原子的杂化轨道类型;元素的非金属性越强,其电负性越大;
(2)①核外电子排布相同的离子,核电荷数越大,离子半径越小;
②该元素的第III电离能剧增,则该元素属于第IIA族;
(3)NaH具有NaCl型晶体结构,食盐晶体里Na+和Cl-的间距为棱长的一半,据此分析解答.
解答 解:(1)①基态Cl原子中电子占据的最高能层为第3能层,符号M,该能层有1个s轨道、3个p轨道、5个d轨道,共有9 个原子轨道,
故答案为:M;9;
②BH4-中B原子价层电子数=4+$\frac{1}{2}$=4,B原子的杂化轨道类型是sp3杂化,且不含孤电子对,所以是正四面体构型,非金属的非金属性越强其电负性越大,非金属性最强的是H元素,其次是B元素,最小的是Li元素,所以Li、B、H元素的电负性由大到小排列顺序为H>B>Li,
故答案为:正四面体;sp3;H>B>Li;
(2)①核外电子排布相同,核电荷数越大,离子半径越小,锂的质子数为3,氢的质子数为1,Li+、H-核外电子数都为2,所以半径Li+<H-,
故答案为:<;
②该元素的第III电离能剧增,则该元素属于第IIA族,为Mg元素,
故答案为:Mg;
(3)NaH具有NaCl型晶体结构,NaH晶体的晶胞参数a=488pm(棱长),Na+半径为102pm,H-的半径为$\frac{488-102×2}{2}$=142pm,该晶胞中钠离子个数=8×$\frac{1}{8}$+6×$\frac{1}{2}$=4,氢离子个数=12×$\frac{1}{4}$+1=4,NaH的理论密度是ρ=$\frac{4M}{{N}_{A}V}$=$\frac{24×4}{{N}_{A}×48{8}^{3}×1{0}^{-30}}$,
故答案为:142pm; $\frac{24×4}{{N}_{A}×48{8}^{3}×1{0}^{-30}}$.
点评 本题考查物质结构和性质,涉及核外电子排布、杂化方式的判断、空间构型的判断、晶胞的计算等知识点,难点是晶胞的计算,灵活运用公式是解本题关键,难度中等.

 阅读快车系列答案
阅读快车系列答案| 选项 | 实验操作 | 现象 | 结论 |
| A | SO2通入足量的稀Fe(NO3)3溶液 | 溶液由棕黄色变为浅绿色,但立即又变成棕黄色 | 氧化性:HNO3>稀硫酸>Fe3+ |
| B | 相同条件下,测定等浓度的Na2CO3和Na2SO3溶液的pH | 前者pH比后者的大 | 非金属性:S>C |
| C | 将表面氧化的铜丝从酒精灯的外焰慢慢移向内焰 | 黑色的铜丝变红色 | 氧化铜被酒精灯内焰的乙醇蒸汽还原 |
| D | 取适量NH4Al(SO4)2样品置于试管中加水溶解,滴加少量稀NaOH溶液 | 湿润的红色石蕊试纸靠近试管口,试纸变蓝 | NH4Al(SO4)2溶液中存在NH4+ |
| A. | A | B. | B | C. | C | D. | D |
| A. | “霾尘积聚难见路人”,雾霾所形成的气溶胶有丁达尔效应 | |
| B. | “熬胆矾铁釜,久之亦化为铜”,该过程发生了置换反应 | |
| C. | “青蒿一握,以水二升渍,绞取汁”,屠呦呦对青蒿素的提取属于化学变化 | |
| D. | 古剑“沈卢”“以剂钢为刃,柔铁为茎干,不尔则多断折”,剂钢指的是铁的合金 |
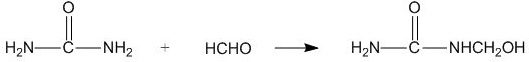
(尿素)
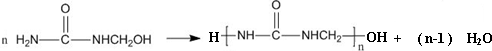
(电玉)
| A. | 合成脲醛塑料的反应为加聚反应 | |
| B. | 尿素与氰酸铵 ( NH4CNO ) 互为同系物 | |
| C. | 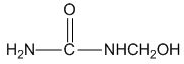 能发生水解反应 能发生水解反应 | |
| D. | 脲醛塑料平均相对分子质量为10000,平均聚合度为111 |
| A. | 苯、氯乙烯、丙烯分子中所有原子均在同一平面 | |
| B. | 汽油、柴油、植物油都是碳氢化合物 | |
| C. | 甲烷、乙烷、丙烷在光照下分别与氯气反应,生成的一氯代物都只有一种 | |
| D. | 乙醇、甲苯和溴苯可用水鉴别 |
| A. |  验证沉淀转化 | B. |  除去苯中的苯酚 | ||
| C. |  观察铁的吸氧腐蚀 | D. |  检验乙炔的还原性 |
| A. | B的单质在自然界只有一种核素 | |
| B. | 元素C、D、E的简单离子的半径依次减小 | |
| C. | E的单质氧化性最强 | |
| D. | 化合物AE与CE含有相同类型的化学键 |



