题目内容
对下列实验的现象描述正确的是( )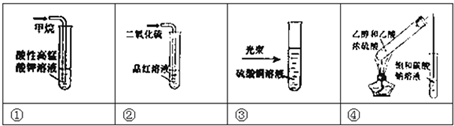

| A、实验①溶液褪色 |
| B、实验③溶液中看到一条光亮的通路 |
| C、实验②溶液褪色 |
| D、实验④饱和碳酸钠溶液下方出现油状液体 |
考点:化学实验方案的评价
专题:实验评价题
分析:A.甲烷性质稳定;
B.溶液无丁达尔效应;
C.二氧化硫有漂白性;
D.乙酸乙酯的密度比水小.
B.溶液无丁达尔效应;
C.二氧化硫有漂白性;
D.乙酸乙酯的密度比水小.
解答:
解:A.甲烷性质稳定,不与酸性高锰酸钾溶液反应,故A错误;
B.硫酸铜溶液无丁达尔效应,故B错误;
C.二氧化硫有漂白性,能使品红褪色,故C正确;
D.乙酸乙酯的密度比水小,位于上方,故D错误.
故选C.
B.硫酸铜溶液无丁达尔效应,故B错误;
C.二氧化硫有漂白性,能使品红褪色,故C正确;
D.乙酸乙酯的密度比水小,位于上方,故D错误.
故选C.
点评:本题考查化学实验方案的评价,为高频考点,涉及物质制备、性质以及胶体的性质等,侧重实验基本操作和实验原理的考查,注意装置的作用及实验的操作性、评价性分析,题目难度不大.

练习册系列答案
相关题目
下列叙述正确的是( )
| A、将稀氨水逐滴加入稀硫酸中,当溶液pH=7时,c(SO42-)>c(NH4+) | ||
| B、两种醋酸溶液的物质的量浓度分别为c1和c2,pH分别为a和a+1,则c1=10c2 | ||
| C、某种物质溶于水形成酸性溶液,该物质可能是强酸与强碱反应形成的盐 | ||
D、向0.1 mol/L的氨水中加入少量硫酸铵固体,则溶液中
|
 新华网2005年4月2日讯:美国研究人员在网络版《科学》杂志上发表论文说,他们开发出了一种新的固体氧化物燃料电池,在用碳氢化合物--异辛烷做燃料时,能源转换效率有望达到50%.采用异辛烷(iso-C8H18)的新型固体氧化物燃料电池,相当于把氧的提纯工厂“压缩”在一个小型装置中,而且异辛烷属于直链烃类,与汽油非常类似,不需要新建基础设施,因此这种燃料电池的前景非常可观.已知该电池的原理结构如图所示,中间阴影部分为固体氧化物陶瓷,可传递氧离子,下列有关说法错误的是( )
新华网2005年4月2日讯:美国研究人员在网络版《科学》杂志上发表论文说,他们开发出了一种新的固体氧化物燃料电池,在用碳氢化合物--异辛烷做燃料时,能源转换效率有望达到50%.采用异辛烷(iso-C8H18)的新型固体氧化物燃料电池,相当于把氧的提纯工厂“压缩”在一个小型装置中,而且异辛烷属于直链烃类,与汽油非常类似,不需要新建基础设施,因此这种燃料电池的前景非常可观.已知该电池的原理结构如图所示,中间阴影部分为固体氧化物陶瓷,可传递氧离子,下列有关说法错误的是( )| A、异辛烷和氧气不需要储存在电池内,可减小电池的体积 |
| B、氢燃料电池的优点是实现零排放,缺点是氢难以制得,同时氢的提纯和储存也较为困难 |
| C、原电池负极的电极反应式为2C8H18+50O2--100e-═16CO2+18H2O |
| D、通异辛烷的电极为电池的正极 |
在100mL 0.1mol/L的MgCl2溶液中Cl-的物质的量浓度为( )
| A、0.01mol/L |
| B、0.02mol/L |
| C、0.1 mol/L |
| D、0.2 mol/L |
下列关于淀粉的说法不正确的是( )
| A、淀粉不溶于水 |
| B、淀粉属于高分子化合物 |
| C、淀粉在人体内能够水解 |
| D、淀粉与碘作用呈蓝色 |
下列排序正确的是( )
| A、酸性:H2CO3<C6H5OH<H3COOH |
| B、沸点:PH3<NH3<H2O |
| C、熔点:MgBr2<CCl4<BN |
| D、碱性:Ba(OH)2<Ca(OH)2<KOH |
下列物质中既有离子键,又有共价键的是( )
| A、H2O |
| B、CaCl2 |
| C、NH4NO3 |
| D、Cl2 |
