题目内容
下列离子能大量共存,且满足相应要求的是( )
| 选项 | 离子 | 要求 | ||||
| A | NH
| 滴加NaOH浓溶液立刻有气体产生 | ||||
| B | K+、NO
| c(K+)<c(Cl-) | ||||
| C | Fe2+、NO
| 逐滴滴加盐酸时溶液有颜色变化 | ||||
| D | Na+、HCO
| 逐滴滴加氨水立即有沉淀产生 |
| A、A | B、B | C、C | D、D |
考点:离子共存问题
专题:离子反应专题
分析:A.酸性条件下滴加NaOH溶液时,先发生中和反应;
B.溶液呈电中性,溶液中阴阳离子所带电荷相等;
C.酸性条件下,亚铁离子能被硝酸根离子氧化生成铁离子;
D.滴加氨水时,镁离子和氢氧根离子反应生成沉淀.
B.溶液呈电中性,溶液中阴阳离子所带电荷相等;
C.酸性条件下,亚铁离子能被硝酸根离子氧化生成铁离子;
D.滴加氨水时,镁离子和氢氧根离子反应生成沉淀.
解答:
解:A.酸性条件下滴加NaOH溶液时,先发生中和反应,所以不是立刻产生气体,故A错误;
B.溶液呈电中性,溶液中阴阳离子所带电荷相等,所以c(K+)>c(Cl-),故B错误;
C.酸性条件下,亚铁离子能被硝酸根离子氧化生成铁离子,溶液由浅绿色变为黄色,所以有颜色变化,故C正确;
D.滴加氨水时,镁离子和氢氧根离子反应生成白色氢氧化镁沉淀,故D正确;
故选CD.
B.溶液呈电中性,溶液中阴阳离子所带电荷相等,所以c(K+)>c(Cl-),故B错误;
C.酸性条件下,亚铁离子能被硝酸根离子氧化生成铁离子,溶液由浅绿色变为黄色,所以有颜色变化,故C正确;
D.滴加氨水时,镁离子和氢氧根离子反应生成白色氢氧化镁沉淀,故D正确;
故选CD.
点评:本题考查离子共存,为考试热点,注意明确离子不能大量共存的一般情况:能发生复分解反应的离子之间;能发生氧化还原反应的离子之间;能发生络合反应的离子之间(如 Fe3+和 SCN-)等;解决离子共存问题时还应该注意题目所隐含的条件,如:溶液的酸碱性,据此来判断溶液中是否有大量的 H+或OH-;易错选项是C,酸性条件下硝酸根离子才有氧化性,为易错点.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
下列说法正确的是( )
| A、构成原电池正极和负极的材料必须是金属 |
| B、在原电池中,电子流出的一极是负极,该电极被还原 |
| C、实验室欲快速制取氢气,可利用粗锌与稀硫酸反应 |
| D、原电池可以把物质内部的能量全部转化为电能 |
下列变化不属于水解反应的是( )
| A、吃馒头时多咀嚼后有甜味 |
| B、不慎将浓硝酸沾到皮肤上会出现黄色斑痕 |
| C、油脂和氢氧化钠溶液共热后可制得肥皂 |
| D、蛋白质在胃蛋白酶或胰蛋白酶作用下转变为氨基酸 |
一块金属钠投入过量的AlCl3溶液中,生成物是( )
| A、Al、NaCl |
| B、H2、Al(OH)3 |
| C、H2、NaCl、NaAlO2 |
| D、H2、NaCl、Al(OH)3 |
在人类认识、研究有机物方面,化学家们不断探索,做出了不可磨灭的贡献.下列说法不正确的是( )
| A、化学家贝采里乌斯合成了醋酸,首次打破了有机物和无机物的界限 |
| B、化学家李比希用燃烧法来测定有机化合物中碳氢元素质量分数 |
| C、甲烷与氯气的反应属于自由基型链反应 |
| D、化学家海维西运用同位素示踪法来研究有机化学反应历程,获得诺贝尔化学奖 |
下列是有关实验操作的步骤和做法,不正确的是( )
| A、粗盐提纯中除泥沙的操作顺序是:溶解、过滤、蒸发 |
| B、萃取操作时,所选萃取剂的密度没有特别限制 |
| C、蒸馏操作时,冷凝管从上面进水,从下面出水 |
| D、分液操作时,分液漏斗中下层液体从下口放出,上层液体从上口倒出 |
对下列实验的现象描述正确的是( )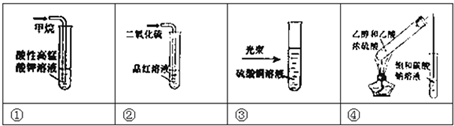

| A、实验①溶液褪色 |
| B、实验③溶液中看到一条光亮的通路 |
| C、实验②溶液褪色 |
| D、实验④饱和碳酸钠溶液下方出现油状液体 |
下列离子方程式书写正确的是( )
| A、明矾溶液中加入过量的氨水A13++4NH3?H20=AlO2-+4NH4++2H2O | ||
| B、在FeI2溶液中滴入少量溴水2Fe2++4I-+3Br2=2Fe3++2I2+6Br- | ||
C、碳酸钠溶液中逐滴加入与之等物质的量的盐酸:CO
| ||
| D、乙酸溶液中加入少量碳酸氢铵溶液CH3COOH+HCO3-=CH3COO-+CO2↑+H2O |