题目内容
下列叙述正确的是( )
| A、将稀氨水逐滴加入稀硫酸中,当溶液pH=7时,c(SO42-)>c(NH4+) | ||
| B、两种醋酸溶液的物质的量浓度分别为c1和c2,pH分别为a和a+1,则c1=10c2 | ||
| C、某种物质溶于水形成酸性溶液,该物质可能是强酸与强碱反应形成的盐 | ||
D、向0.1 mol/L的氨水中加入少量硫酸铵固体,则溶液中
|
考点:弱电解质在水溶液中的电离平衡
专题:电离平衡与溶液的pH专题
分析:A、根据溶液中的电荷守恒分析;
B、醋酸的浓度越小电离程度越大;
C、二元强酸的酸式盐的水溶液显酸性;
D、增大铵根离子浓度会抑制一水合氨的电离.
B、醋酸的浓度越小电离程度越大;
C、二元强酸的酸式盐的水溶液显酸性;
D、增大铵根离子浓度会抑制一水合氨的电离.
解答:
解:A、将稀氨水逐滴加入稀硫酸中,当溶液pH=7时,溶液中的电荷守恒为2c(SO42-)+c(OH-)=c(NH4+)+c(H+),pH=7说明c(OH-)=+c(H+),则2c(SO42-)=c(NH4+),故A错误;
B、醋酸的浓度越小电离程度越大,两种醋酸溶液的物质的量浓度分别为c1和c2,pH分别为a和a+1,则c2浓度的醋酸的电离程度较大,所以则c1>10c2,故B错误;
C、二元强酸的酸式盐的水溶液显酸性,则某种物质溶于水形成酸性溶液,该物质可能是强酸与强碱反应形成的盐,如氢氧化钠与硫酸形成NaHSO4,故C正确;
D、向0.1 mol/L的氨水中加入少量硫酸铵固体,铵根离子浓度增大,抑制一水合氨的电离,则c(OH-)减小,c(NH3?H2O)增大,所以溶液中
减小,故D错误.
故选C.
B、醋酸的浓度越小电离程度越大,两种醋酸溶液的物质的量浓度分别为c1和c2,pH分别为a和a+1,则c2浓度的醋酸的电离程度较大,所以则c1>10c2,故B错误;
C、二元强酸的酸式盐的水溶液显酸性,则某种物质溶于水形成酸性溶液,该物质可能是强酸与强碱反应形成的盐,如氢氧化钠与硫酸形成NaHSO4,故C正确;
D、向0.1 mol/L的氨水中加入少量硫酸铵固体,铵根离子浓度增大,抑制一水合氨的电离,则c(OH-)减小,c(NH3?H2O)增大,所以溶液中
| c(OH)- |
| c(NH3?H2O) |
故选C.
点评:本题考查了弱电解质的电离、盐的水解,注意把握影响弱电解质的电离和盐的水解的因素,明确溶液中的守恒关系,题目难度不大.

练习册系列答案
 新思维假期作业寒假吉林大学出版社系列答案
新思维假期作业寒假吉林大学出版社系列答案
相关题目
今有一混合物的水溶液,只可能含有以下离子中的若干种:K+、NH4+、Cl-、Mg2+、Ba2+、CO32-、SO42-,现取三份100mL溶液进行如下实验:
(1)第一份加入AgNO3溶液有沉淀产生
(2)第二份加足量NaOH溶液加热后,收集到气体0.06mol
(3)第三份加足量BaCl2溶液后,得干燥沉淀6.27g,经足量盐酸洗涤、干燥后,沉淀质量为2.33g.
根据上述实验,以下推测正确的是( )
(1)第一份加入AgNO3溶液有沉淀产生
(2)第二份加足量NaOH溶液加热后,收集到气体0.06mol
(3)第三份加足量BaCl2溶液后,得干燥沉淀6.27g,经足量盐酸洗涤、干燥后,沉淀质量为2.33g.
根据上述实验,以下推测正确的是( )
| A、K+一定存在 |
| B、100mL溶液中含0.01 mol CO32- |
| C、Ba2+一定不存在,Mg2+可能存在 |
| D、K+、Cl-可能存在 |
下列实验对应的结论正确的是( )
| A | B | C | D | |
| 装置 | 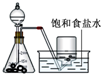 |  |  | 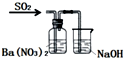 洗气瓶中产生白色沉淀 |
| 结论 | 用浓盐酸与高锰酸钾制氯气 | 能证明非金属性 Cl>C>Si | 分离出Cl2与KI溶液反应生成的碘 | 白色沉淀是BaSO3 |
| A、A | B、B | C、C | D、D |
下列说法正确的是( )
| A、含有氧元素的化合物一定是氧化物 |
| B、在水溶液中能电离出H+的化合物一定是酸 |
| C、盐一定是有金属阳离子和酸根离子构成 |
| D、HCl不导电 |
下列反应的离子方程式正确的是( )
| A、Ba(OH)2溶液中加入少量KAl(SO4)2溶液:3Ba2++6OH-+2Al3++3SO42-═BaSO4↓+2Al(OH)3↓ |
| B、FeCl3溶液中加入过量Na2S溶液:2Fe3++S2-═2Fe2++S↓ |
| C、将适量SO2通入Ca(ClO)2溶液中 Ca2++2ClO-+SO2+H2O═CaSO3↓+2HClO |
| D、向Ca(OH)2溶液中加入过量的NaHCO3溶液 Ca2++2HCO3-+2OH-═CO32-+CaCO3↓+2H2O |
下列说法正确的是( )
| A、构成原电池正极和负极的材料必须是金属 |
| B、在原电池中,电子流出的一极是负极,该电极被还原 |
| C、实验室欲快速制取氢气,可利用粗锌与稀硫酸反应 |
| D、原电池可以把物质内部的能量全部转化为电能 |
下列变化不属于水解反应的是( )
| A、吃馒头时多咀嚼后有甜味 |
| B、不慎将浓硝酸沾到皮肤上会出现黄色斑痕 |
| C、油脂和氢氧化钠溶液共热后可制得肥皂 |
| D、蛋白质在胃蛋白酶或胰蛋白酶作用下转变为氨基酸 |
对下列实验的现象描述正确的是( )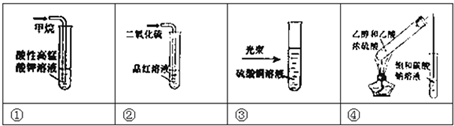

| A、实验①溶液褪色 |
| B、实验③溶液中看到一条光亮的通路 |
| C、实验②溶液褪色 |
| D、实验④饱和碳酸钠溶液下方出现油状液体 |