题目内容
 合成氨技术的创立开辟了人工固氮的重要途径,其研究来自正确的理论指导,合成氨反应的平衡常数K值和温度的关系如下:
合成氨技术的创立开辟了人工固氮的重要途径,其研究来自正确的理论指导,合成氨反应的平衡常数K值和温度的关系如下:| 温 度(℃) | 360 | 440 | 520 |
| K值 | 0.036 | 0.010 | 0.0038 |
①写出工业合成氨的化学反应的平衡常数K值表达式为
②由上表数据可知该反应为
③理论上,为了增大平衡时H2的转化率,可采取的措施是
a.增大压强 b.使用合适的催化剂
c.升高温度 d.及时分离出产物中的NH3
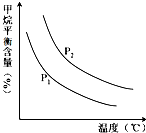
(2)原料气H2可通过反应 CH4(g)+H2O (g)═CO(g)+3H2(g) 获取,已知该反应中,当初始混合气中的
| n(H2O) |
| n(CH4) |
①图中,两条曲线表示压强的关系是:P1
②该反应为
(3)原料气H2还可通过反应CO(g)+H2O(g)═CO2 (g)+H2(g) 获取.
①T℃时,向容积固定为5L的容器中充入1mol水蒸气和1mol CO,反应达平衡后,测得CO的浓度为0.08mol?L-1,则该温度下反应的平衡常数K值为
②保持温度仍为T℃,改变水蒸气和CO的初始物质的量之比,充入容器进行反应,下列描述能够说明体系处于平衡状态的是
a.容器内压强不随时间改变
b.混合气体的密度不随时间改变
c.单位时间内生成amolCO2的同时消耗amolH2
d.混合气中n(CO):n(H2O):n(CO2):n(H2)=1:16:6:6.
考点:化学平衡常数的含义,化学平衡的影响因素,化学平衡状态的判断,产物的百分含量随浓度、时间的变化曲线
专题:化学平衡专题
分析:(1)①依据合成氨的化学方程式书写平衡常数表达式,用生成物平衡浓度幂次方乘积除以反应物平衡浓度幂次方乘积;
②分析平衡常数随温度变化结合平衡移动原理判断;
③为了增大平衡时H2的转化率,平衡正向进行分析选项;
(2)①依据图象变化分析,相同温度下,CH4(g)+H2O (g)═CO(g)+3H2(g),反应是气体体积增大的反应,压强越大,平衡逆向进行,甲烷平衡含量越高;
②压强一定,温度升高,甲烷平衡含量减小,平衡正向进行,依据平衡移动原理分析判断;
(3)①依据化学平衡三段式列式计算平衡浓度,结合平衡常数概念计算得到;
②化学平衡状态,反应的正逆反应速率相同,各成分含量保持不变分析选项.
②分析平衡常数随温度变化结合平衡移动原理判断;
③为了增大平衡时H2的转化率,平衡正向进行分析选项;
(2)①依据图象变化分析,相同温度下,CH4(g)+H2O (g)═CO(g)+3H2(g),反应是气体体积增大的反应,压强越大,平衡逆向进行,甲烷平衡含量越高;
②压强一定,温度升高,甲烷平衡含量减小,平衡正向进行,依据平衡移动原理分析判断;
(3)①依据化学平衡三段式列式计算平衡浓度,结合平衡常数概念计算得到;
②化学平衡状态,反应的正逆反应速率相同,各成分含量保持不变分析选项.
解答:
解:(1)①合成氨的化学方程式为N2+3H2
2NH3,用生成物平衡浓度幂次方乘积除以反应物平衡浓度幂次方乘积书写平衡常数表达式K=
;
故答案为:
;
②图表中平衡常数随温度升高减小,说明平衡逆向进行,逆向是吸热反应,正向是放热反应;
故答案为:放热;
③反应是N2+3H2
2NH3,反应是气体体积减小的放热反应,为了增大平衡时H2的转化率,平衡正向进行分析,
a.增大压强,平衡正向进行,氢气转化率增大,故a符合;
b.使用合适的催化剂,改变反应速率,不能改变平衡,氢气转化率不变,故b不符合;
c.升高温度平衡逆向进行,氢气转化率减小,故c不符合;
d.及时分离出产物中的NH3,平衡正向进行,氢气转化率增大,故d符合;
故答案为:ad;
(2)①依据图象变化分析,相同温度下,CH4(g)+H2O (g)═CO(g)+3H2(g),反应是气体体积增大的反应,压强越大,平衡逆向进行,甲烷平衡含量越高,所以P2>P1;故答案为:<;
②压强一定,温度升高,甲烷平衡含量减小,平衡正向进行,正反应为吸热反应;
故答案为:吸热;
(3)①依据化学平衡三段式列式计算平衡浓度,℃时,向容积固定为5L的容器中充入1mol水蒸气和1mol CO,反应达平衡后,测得CO的浓度为0.08mol?L-1,
CO(g)+H2O(g)═CO2 (g)+H2(g)
起始量(mol/L) 0.2 0.2 0 0
变化量(mol/L) 0.12 0.12 0.12 0.12
平衡量(mol/L) 0.08 0.08 0.12 0.12
则该温度下反应的平衡常数K=
=2.25
故答案为:2.25;
②化学平衡状态,反应的正逆反应速率相同,各成分含量保持不变分析选项,CO(g)+H2O(g)═CO2 (g)+H2(g),反应是气体体积不变反应;
a.反应过程中和平衡状态下压强相同,容器内压强不随时间改变,不能说明反应达到平衡状态,故a不符合;
b.混合气体质量守恒,反应前后气体体积不变,反应过程中和平衡状态下,混合气体的密度不随时间改变,不能说明反应达到平衡状态,故b不符合;
c.单位时间内生成amolCO2的同时消耗amolH2,说明二氧化碳或氢气的正逆反应速率相同,说明反应达到平衡状态,故c符合;
d.混合气中n(CO):n(H2O):n(CO2):n(H2)=1:16:6:6,依据反应前后气体物质的量相同,可以利用物质的量代替浓度计算浓度商和平衡常数比较,
Q=
2.25=K,说明反应达到平衡状态,故d符合;
故答案为:cd.
| ||
| 高温高压 |
| c2(NH3) |
| c(N2)c3(H2) |
故答案为:
| c2(NH3) |
| c(N2)c3(H2) |
②图表中平衡常数随温度升高减小,说明平衡逆向进行,逆向是吸热反应,正向是放热反应;
故答案为:放热;
③反应是N2+3H2
| ||
| 高温高压 |
a.增大压强,平衡正向进行,氢气转化率增大,故a符合;
b.使用合适的催化剂,改变反应速率,不能改变平衡,氢气转化率不变,故b不符合;
c.升高温度平衡逆向进行,氢气转化率减小,故c不符合;
d.及时分离出产物中的NH3,平衡正向进行,氢气转化率增大,故d符合;
故答案为:ad;
(2)①依据图象变化分析,相同温度下,CH4(g)+H2O (g)═CO(g)+3H2(g),反应是气体体积增大的反应,压强越大,平衡逆向进行,甲烷平衡含量越高,所以P2>P1;故答案为:<;
②压强一定,温度升高,甲烷平衡含量减小,平衡正向进行,正反应为吸热反应;
故答案为:吸热;
(3)①依据化学平衡三段式列式计算平衡浓度,℃时,向容积固定为5L的容器中充入1mol水蒸气和1mol CO,反应达平衡后,测得CO的浓度为0.08mol?L-1,
CO(g)+H2O(g)═CO2 (g)+H2(g)
起始量(mol/L) 0.2 0.2 0 0
变化量(mol/L) 0.12 0.12 0.12 0.12
平衡量(mol/L) 0.08 0.08 0.12 0.12
则该温度下反应的平衡常数K=
| 0.12×0.12 |
| 0.08×0.08 |
故答案为:2.25;
②化学平衡状态,反应的正逆反应速率相同,各成分含量保持不变分析选项,CO(g)+H2O(g)═CO2 (g)+H2(g),反应是气体体积不变反应;
a.反应过程中和平衡状态下压强相同,容器内压强不随时间改变,不能说明反应达到平衡状态,故a不符合;
b.混合气体质量守恒,反应前后气体体积不变,反应过程中和平衡状态下,混合气体的密度不随时间改变,不能说明反应达到平衡状态,故b不符合;
c.单位时间内生成amolCO2的同时消耗amolH2,说明二氧化碳或氢气的正逆反应速率相同,说明反应达到平衡状态,故c符合;
d.混合气中n(CO):n(H2O):n(CO2):n(H2)=1:16:6:6,依据反应前后气体物质的量相同,可以利用物质的量代替浓度计算浓度商和平衡常数比较,
Q=
| 6×6 |
| 1×16 |
故答案为:cd.
点评:本题考查了化学平衡影响因素,平衡标志分析,平衡常数的计算应用,主要是图象分析判断,平衡移动原理的理解应用,掌握基础是关键,题目难度中等.

练习册系列答案
 名师点拨卷系列答案
名师点拨卷系列答案 英才计划期末调研系列答案
英才计划期末调研系列答案
相关题目
用NA代表阿伏加德罗常数的值,下列说法正确的是( )
| A、常温下,pH=7的任何溶液中含有OH-数目均为10-7NA |
| B、23g乙醇中含有C-H键的数目为3NA |
| C、4.8g O2和O3以任何比例组成的混合气体中含有的氧原子数目均为0.3NA |
| D、常温常压下,2.24L Cl2与足量铁粉充分反应,转移的电子数目为0.2NA |
下列说法中不正确的是( )
| A、1mol 氧气中含有12.04×1023个氧原子,在标准状况下占有体积22.4 L |
| B、等体积、浓度均为1mol/L的碳酸和盐酸,电离出的氢离子数之比为2:1 |
| C、1mol臭氧和1.5mol氧气含有相同的氧原子数 |
| D、等物质的量的干冰和葡萄糖(C6H12O6)中所含氧原子数之比为1:3 |
H2A是一种弱酸,已知常温下0.1mol/L NaHA溶液呈酸性.关于该溶液中微粒浓度的以下判断中,可能错误的是( )
| A、c(A2-)+c(OH-)=c(H2A)+c(H+) |
| B、c(HA-)>c(A2-)>c(H2A) |
| C、c(HA-)>c(H+)>c(OH-) |
| D、c(HA-)>c(OH-)>c(A2-) |
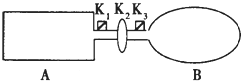 A是由导热材料制成的密闭容器,B是一耐化学腐蚀且易传热的气球.关闭K2,将等量且少量的NO2通过K1、K3分别充人A、B中,反应起始时,A、B的体积均为V L.
A是由导热材料制成的密闭容器,B是一耐化学腐蚀且易传热的气球.关闭K2,将等量且少量的NO2通过K1、K3分别充人A、B中,反应起始时,A、B的体积均为V L.