题目内容
 温州某学生用0.1000mol/L NaOH溶液滴定未知浓度的盐酸溶液,其操作可分解为如下几步:
温州某学生用0.1000mol/L NaOH溶液滴定未知浓度的盐酸溶液,其操作可分解为如下几步:A.检查滴定管是否漏水
B.用蒸馏水洗干净滴定管
C.取下碱式滴定管用标准的NaOH溶液润洗后,将标准液注入碱式滴定管“0”刻度以上2~3cm处,再把碱式滴定管固定好,调节液面至“0”刻度或“0”刻度以下
D.用待测定的溶液润洗酸式滴定管
E.用酸式滴定管取稀盐酸20.00mL,注入锥形瓶中,加入酚酞
F.把锥形瓶放在滴定管下面,瓶下垫一张白纸,边滴边摇动锥形瓶直至滴定终点,记下滴定管液面所在刻度
G.另取锥形瓶,再重复操作一次
完成以下填空:
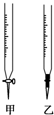
(1)操作F中应该选择图中
(2)滴定时边滴边摇动锥形瓶,眼睛应观察
A.滴定管内液面的变化 B.锥形瓶内溶液颜色的变化
滴定终点溶液颜色的变化是
(3)滴定结果如表所示:
| 滴定次数 | 待测液体积/mL | 标准溶液的体积/mL | ||
| 滴定前刻度 | 滴定后刻度 | |||
| 1 | 20 | 1.02 | 21.03 | |
| 2 | 20 | 2.00 | 25.00 | |
| 3 | 20 | 0.60 | 20.59 | |
A.碱式滴定管在装液前未用标准NaOH溶液润洗2~3次
B.滴定开始前碱式滴定管尖嘴部分有气泡,在滴定终点读数时未发现气泡
C.滴定开始前碱式滴定管尖嘴部分没有气泡,在滴定终点读数时发现尖嘴部分有气泡
D.达到滴定终点时,仰视溶液凹液面最低点读数
E.滴定过程中,锥形瓶摇荡得太剧烈,以致有些液滴飞溅出来
(4)该盐酸的浓度为
(5)如果准确移取20.00mL 0.1000mol/L NaOH溶液于锥形瓶中,滴入酚酞指示剂,然后用未知浓度的盐酸(装在酸式滴定管中)滴定,是否也可测定出盐酸的物质的量浓度?
考点:中和滴定
专题:实验题
分析:(1)用碱式滴定管盛装KOH溶液;
(2)实验中应控制流速并观察锥形瓶中颜色变化;如溶液颜色变化且半分钟内不变色,可说明达到滴定终点,甲基橙在酸性环境中为红色,中性环境中为橙色;
(3)第二次实验有误差,NaOH溶液体积比第一次和第三次大太多;
(4)先判断数据的有效性,然后求出平均值,最后根据关系式HCl~NaOH来计算出盐酸的浓度;
(5)根据关系式HCl~NaOH来计算出盐酸的浓度.
(2)实验中应控制流速并观察锥形瓶中颜色变化;如溶液颜色变化且半分钟内不变色,可说明达到滴定终点,甲基橙在酸性环境中为红色,中性环境中为橙色;
(3)第二次实验有误差,NaOH溶液体积比第一次和第三次大太多;
(4)先判断数据的有效性,然后求出平均值,最后根据关系式HCl~NaOH来计算出盐酸的浓度;
(5)根据关系式HCl~NaOH来计算出盐酸的浓度.
解答:
解:(1)滴定管乙下端是橡皮管,为碱式滴定管,故答案为:乙;
(2)滴定时边滴边摇动锥形瓶,眼睛应观察锥形瓶中颜色变化,无色变浅红色且半分钟内不褪色,可说明达到滴定终点;甲基橙在酸性环境中为红色,滴定终点为中性环境,甲基橙变为橙色,故答案为:B;无色变浅红色且半分钟内不褪色;红色变橙色;
(3)第二次实验有误差,NaOH溶液体积比第一次和第三次大太多,
A、碱式滴定管在装液前未用标准NaOH溶液润洗,导致浓度降低,所用所用溶液体积偏大,故A正确;
B、滴定开始前碱式滴定管尖嘴部分有气泡,在滴定终点读数时未发现气泡,导致所用溶液体积偏大,故B正确;
C、滴定开始前碱式滴定管尖嘴部分没有气泡,在滴定终点读数时发现尖嘴部分有气泡,导致所用溶液体积偏小,故C错误;
D、达到滴定终点时,仰视溶液凹液面最低点读数,导致读数偏大,故D正确;
E、滴定过程中,锥形瓶摇荡得太剧烈,以致有些液滴飞溅出来,导致所用溶液体积偏小,故E错误;
故答案为:2;ABD;
(4)数据2无效,取1、3体积进行计算,所用标准液的平均体积为21.03mL-1.02mL+20.59mL-0.60mL2mL=20.00mL,
HCl~NaOH
1 1
C(HCl)×20.00mL 0.1000mol/L×20.00mL;
C(HCl)=0.1000mol/L×20.00mL20.00mL=0.1000mol/L,故答案为:0.1000;
(5)准确移取20.00mL 0.1000mol/L NaOH溶液于锥形瓶中,滴入酚酞指示剂,然后用未知浓度的盐酸(装在酸式滴定管中)滴定,通过盐酸的体积,根据HCl~NaOH来计算出盐酸的浓度,故答案为:是.
(2)滴定时边滴边摇动锥形瓶,眼睛应观察锥形瓶中颜色变化,无色变浅红色且半分钟内不褪色,可说明达到滴定终点;甲基橙在酸性环境中为红色,滴定终点为中性环境,甲基橙变为橙色,故答案为:B;无色变浅红色且半分钟内不褪色;红色变橙色;
(3)第二次实验有误差,NaOH溶液体积比第一次和第三次大太多,
A、碱式滴定管在装液前未用标准NaOH溶液润洗,导致浓度降低,所用所用溶液体积偏大,故A正确;
B、滴定开始前碱式滴定管尖嘴部分有气泡,在滴定终点读数时未发现气泡,导致所用溶液体积偏大,故B正确;
C、滴定开始前碱式滴定管尖嘴部分没有气泡,在滴定终点读数时发现尖嘴部分有气泡,导致所用溶液体积偏小,故C错误;
D、达到滴定终点时,仰视溶液凹液面最低点读数,导致读数偏大,故D正确;
E、滴定过程中,锥形瓶摇荡得太剧烈,以致有些液滴飞溅出来,导致所用溶液体积偏小,故E错误;
故答案为:2;ABD;
(4)数据2无效,取1、3体积进行计算,所用标准液的平均体积为21.03mL-1.02mL+20.59mL-0.60mL2mL=20.00mL,
HCl~NaOH
1 1
C(HCl)×20.00mL 0.1000mol/L×20.00mL;
C(HCl)=0.1000mol/L×20.00mL20.00mL=0.1000mol/L,故答案为:0.1000;
(5)准确移取20.00mL 0.1000mol/L NaOH溶液于锥形瓶中,滴入酚酞指示剂,然后用未知浓度的盐酸(装在酸式滴定管中)滴定,通过盐酸的体积,根据HCl~NaOH来计算出盐酸的浓度,故答案为:是.
点评:本题考查酸碱中和滴定实验,题目难度不大,注意把握实验的误差分析,把握实验基本操作.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
下列各种醇既可发生消去反应,又可被氧化成相应醛的是( )
| A、CH3OH |
| B、HOCH2CH2CH3 |
| C、CH3CHOHCH3 |
| D、(CH3)3COH |
用盐酸滴定未知浓度的氢氧化钠溶液,下列操作导致结果偏低的是( )
| A、酸式滴定管未用标准盐酸溶液润洗就直接注入标准盐酸溶液 |
| B、滴定前盛放氢氧化钠溶液的锥形瓶用蒸馏水洗净后没有干燥 |
| C、酸式滴定管在滴定前有气泡,滴定后气泡消失 |
| D、读取盐酸体积时,开始仰视读数,滴定结束时平视读数 |
下列关于油脂的叙述不正确的是( )
| A、属于酯类 |
| B、没有固定的熔沸点 |
| C、是高级脂肪酸的甘油酯 |
| D、油脂的氢化属于氧化反应 |
用某种仪器量一液体体积时,平视时读数为nmL,仰视时读数为xmL,俯视时读数为y mL,若x>n>y,则所使用的仪器可能是( )
| A、量筒 | B、酸式滴定管 |
| C、量杯 | D、容量瓶 |
用分液漏斗可以分离的一组物质是( )
| A、苯和醋酸钠溶液 |
| B、苯酚和乙醇 |
| C、乙酸和乙醇 |
| D、植物油和乙酸乙酯 |
将pH=3的盐酸和pH=11的氨水等体积混合,完全反应后溶液中离子浓度的关系正确( )
| A、c(NH4+)>c(Cl-)>c(OH-)>c(H+) |
| B、c(NH4+)>c(Cl-)>c(H+)>c(OH-) |
| C、c(Cl-)>c(NH4+)>c(H+)>c(OH-) |
| D、c(Cl-)>c(NH4+)>c(OH-)>c(H+) |