题目内容
现有以下物质:①NaCl晶体 ②液态HCl ③CaCO3固体 ④熔融KCl ⑤蔗糖 ⑥铜 ⑦CO2⑧H2SO4 ⑨KOH固体
(1)以上物质中能导电的是 .
(2)以上物质中属于电解质的是 ,属于非电解质的是 .
(1)以上物质中能导电的是
(2)以上物质中属于电解质的是
考点:电解质与非电解质
专题:电离平衡与溶液的pH专题
分析:(1)能导电的物质中含有自由移动的阴阳离子或电子,如金属或电解质溶液能导电;
(2)在水溶液里或熔融状态下能导电的化合物是电解质,酸、碱、盐、金属氧化物都属于电解质;在水溶液里和熔融状态下都不导电的化合物是非电解质,非金属氧化物、部分非金属氢化物和大多数有机物属于非电解质;单质和混合物既不是电解质也不是非电解质.
(2)在水溶液里或熔融状态下能导电的化合物是电解质,酸、碱、盐、金属氧化物都属于电解质;在水溶液里和熔融状态下都不导电的化合物是非电解质,非金属氧化物、部分非金属氢化物和大多数有机物属于非电解质;单质和混合物既不是电解质也不是非电解质.
解答:
解:①NaCl晶体 ②液态HCl ③CaCO3固体 ④熔融KCl ⑤蔗糖 ⑥铜 ⑦CO2⑧H2SO4 ⑨KOH固体中分析如下:
①NaCl晶体属于电解质,但无自由移动离子,不能导电;
②液态HCl属于电解质,但不含自由移动的阴、阳离子,所以不导电;
③CaCO3属于电解质,因为不含自由移动的阴、阳离子,所以不导电;
④熔融KCl属于电解质,因为含有自由移动的阴、阳离子,所以能导电;
⑤蔗糖属于非电解质,不含自由移动的阴阳离子或自由电子,所以不导电;
⑥铜是单质,所以既不是电解质也不是非电解质,因为含有自由移动的电子,所以能导电;
⑦CO2属于非电解质,不含自由移动的阴阳离子或自由电子,所以不导电;
⑧H2SO4属于电解质不含自由移动的阴阳离子,不能导电;
⑨KOH固体属于电解质,但没有自由移动的阴、阳离子,所以不导电;
(1)能导电的是④⑥;
故答案为:④⑥;
(2)以上物质中属于电解质的是①②③④⑧⑨;属于非电解质的是⑤⑦.
故答案为:①②③④⑧⑨;⑤⑦.
①NaCl晶体属于电解质,但无自由移动离子,不能导电;
②液态HCl属于电解质,但不含自由移动的阴、阳离子,所以不导电;
③CaCO3属于电解质,因为不含自由移动的阴、阳离子,所以不导电;
④熔融KCl属于电解质,因为含有自由移动的阴、阳离子,所以能导电;
⑤蔗糖属于非电解质,不含自由移动的阴阳离子或自由电子,所以不导电;
⑥铜是单质,所以既不是电解质也不是非电解质,因为含有自由移动的电子,所以能导电;
⑦CO2属于非电解质,不含自由移动的阴阳离子或自由电子,所以不导电;
⑧H2SO4属于电解质不含自由移动的阴阳离子,不能导电;
⑨KOH固体属于电解质,但没有自由移动的阴、阳离子,所以不导电;
(1)能导电的是④⑥;
故答案为:④⑥;
(2)以上物质中属于电解质的是①②③④⑧⑨;属于非电解质的是⑤⑦.
故答案为:①②③④⑧⑨;⑤⑦.
点评:本题考查了物质的导电性、电解质和非电解质的判断,明确物质导电的原因与电解质和非电解质的关系是解本题关键,注意导电的不一定是电解质.

练习册系列答案
 A加金题 系列答案
A加金题 系列答案 全优测试卷系列答案
全优测试卷系列答案
相关题目
下列有关物质用途的说法正确的是( )
| A、单质硅常用做半导体材料和光导纤维,SiO2是人类将光能转化为电能的常用材料 |
| B、纯碱、烧碱、Al(OH)3等常用于治疗胃酸过多 |
| C、H2O2、Na2O2、氯水、漂白粉、84消毒液均可作漂白剂和消毒剂,且它们的漂白原理相同 |
| D、镁铝合金常用于制作窗框是因为它具有坚硬、密度小、溶点高、耐腐蚀等优良性能 |
下列溶液中,各组离子一定能大量共存的是( )
| A、使酚酞试液变红的溶液:Na+、Cl-、SO42-、Fe3+ |
| B、使紫色石蕊试液变红的溶液:Fe2+、Mg2+、NO3-、Cl- |
| C、碳酸氢钠溶液:K+、SO42-、Cl-、H+ |
| D、c(H+)=10-12 mol?L-1的溶液:K+、Ba2+、Cl-、Br- |
 某同学设计了如下方案,来测定过氧化钠的样品的纯度(杂质不参加反应,条件为标准状况).
某同学设计了如下方案,来测定过氧化钠的样品的纯度(杂质不参加反应,条件为标准状况).

 )
)
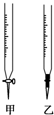 温州某学生用0.1000mol/L NaOH溶液滴定未知浓度的盐酸溶液,其操作可分解为如下几步:
温州某学生用0.1000mol/L NaOH溶液滴定未知浓度的盐酸溶液,其操作可分解为如下几步: