题目内容
25℃时,在1L的密闭容器中充入NO2发生如下反应:2NO2(g)?N2O4(g);△H=-57kJ?mol-1
(1)该反应的△S 0(填“>”、“<”或“=”).
(2)当开始充入0.03mol的NO2时,25℃时,实验测得NO2的平衡浓度为0.01mol?L-1,则NO2的平衡转化率(α)是 .25℃时上述反应的平衡常数K= .
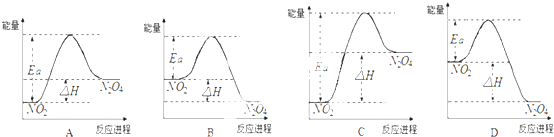
(3)25℃时,实验测得该反应的活化能Ea=92.4kJ?mol-1.下列能量关系图合理的是 .
(1)该反应的△S
(2)当开始充入0.03mol的NO2时,25℃时,实验测得NO2的平衡浓度为0.01mol?L-1,则NO2的平衡转化率(α)是
(3)25℃时,实验测得该反应的活化能Ea=92.4kJ?mol-1.下列能量关系图合理的是

考点:化学平衡的计算,反应热和焓变
专题:
分析:(1)依据反应是气体体积减小的反应判断熵变;
(2)依据化学平衡的三段式列式计算平衡浓度,结合平衡常数、反应物转化率概念计算得到;
(3)依据反应是放热反应,二氧化氮能量高于四氧化二氮分析,结合图象分析活化能数值大于反应焓变判断;
(2)依据化学平衡的三段式列式计算平衡浓度,结合平衡常数、反应物转化率概念计算得到;
(3)依据反应是放热反应,二氧化氮能量高于四氧化二氮分析,结合图象分析活化能数值大于反应焓变判断;
解答:
解:(1)2NO2(g)?N2O4(g)△H=-57kJ?mol-1,依据反应分析可知反应后气体体积减小,所以熵变小于0,△S<0,故答案为:<;
(2)在1L的密闭容器中充入NO2发生如下反应:2NO2(g)?N2O4(g)△H=-57kJ?mol-1,当开始充入0.03mol的NO2时,25℃时,实验测得NO2的平衡浓度为0.01mol?L-1,依据化学平衡三段式列式计算:二氧化氮起始浓度为0.03mol/L,
2NO2(g)?N2O4(g)
起始量(mol/L) 0.03 0
变化量(mol/L) 0.02 0.01
平衡量(mol/L) 0.01 0.01
NO2的平衡转化率(α)=
×100%=66.7%,
平衡常数K=
=
=100L/mol;
故答案为:66.7%;100L/mol;
(3)依据反应是放热反应,二氧化氮能量高于四氧化二氮分析,结合图象分析活化能数值大于反应焓变判断,B符合;AC中二氧化氮能量低于四氧化二氮,错误;D选项活化能数值小于反应焓变,错误;故答案为:B;
(2)在1L的密闭容器中充入NO2发生如下反应:2NO2(g)?N2O4(g)△H=-57kJ?mol-1,当开始充入0.03mol的NO2时,25℃时,实验测得NO2的平衡浓度为0.01mol?L-1,依据化学平衡三段式列式计算:二氧化氮起始浓度为0.03mol/L,
2NO2(g)?N2O4(g)
起始量(mol/L) 0.03 0
变化量(mol/L) 0.02 0.01
平衡量(mol/L) 0.01 0.01
NO2的平衡转化率(α)=
| 0.02mol/L |
| 0.03mol/L |
平衡常数K=
| c(N2O4) |
| c(NO2) |
| 0.01mol/L |
| (0.01mol/L)2 |
故答案为:66.7%;100L/mol;
(3)依据反应是放热反应,二氧化氮能量高于四氧化二氮分析,结合图象分析活化能数值大于反应焓变判断,B符合;AC中二氧化氮能量低于四氧化二氮,错误;D选项活化能数值小于反应焓变,错误;故答案为:B;
点评:本题考查了反应焓变和熵变判断,化学平衡的三段式计算应用,反应为转化率、反应平衡常数概念的计算应用,平衡影响因素的分析判断,题目难度中等.

练习册系列答案
相关题目
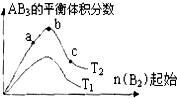 某化学科研小组研究在其他条件不变时,改变某一条件对A2(g)+3B2(g)?2AB3(g)化学平衡状态的影响,得到如下图所示的变化规律(图中T表示温度,n表示物质的量),据此可得出的判断结论不正确的是( )
某化学科研小组研究在其他条件不变时,改变某一条件对A2(g)+3B2(g)?2AB3(g)化学平衡状态的影响,得到如下图所示的变化规律(图中T表示温度,n表示物质的量),据此可得出的判断结论不正确的是( )| A、达到平衡时A2的转化率大小为:c>b>a |
| B、a、b、c三点的平衡常数相同 |
| C、该反应一定是放热反应,且T2<T1 |
| D、b点时,平衡体系中A、B原子数之比一定是1:1 |


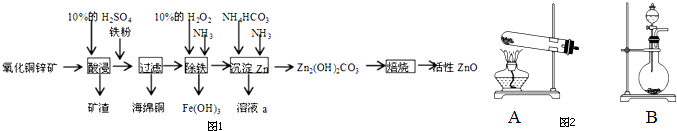
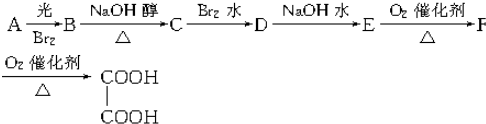
 阅读下列实验内容,根据题目要求回答问题.
阅读下列实验内容,根据题目要求回答问题.