题目内容
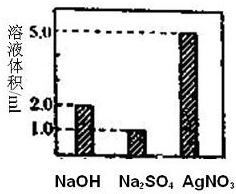
取三份由NaCl、MgCl2、BaCl2溶液组成的营养液各10ml,分别加入1mol?L-1的NaOH、Na2SO4、AgNO3溶液至恰好反应,消耗溶液的体积如图所示,该营养液中钠离子的浓度为( )

| A、0.5 mol?L-1 |
| B、0.1 mol?L-1 |
| C、1 mol?L-1 |
| D、1.5 mol?L-1 |
考点:物质的量浓度的相关计算
专题:计算题
分析:由1mol?L-1的NaOH、Na2SO4、AgNO3溶液至恰好反应分别可以计算出溶液中Mg2+离子的物质的量,Ba2+离子的物质的量和Cl-离子的物质的量,由混合液呈电中性可计算出钠离子的物质的量,从而计算混合溶液中的c(Na+)来解答即可.
解答:
解:由消耗1mol?L-1的NaOH溶液2ml,发生反应为Mg2++2OH-═Mg(OH)2↓,则Mg2+离子的物质的量为
=10-3mol;
由消耗1mol?L-1Na2SO4溶液1ml,发生反应为Ba2++SO42-═BaSO4↓,则Ba2+离子的物质的量为10-3mol;
由消耗1mol?L-1AgNO3溶液5ml,发生反应为Cl-+Ag+═AgCl↓,则Cl-离子的物质的量为5×10-3mol;
设每份中的钠离子的物质的量为x,混合溶液不显电性,
则x+10-3mol×2+10-3mol×2=5×10-3mol,x=10-3mol,则原溶液中的钠离子浓度为c(Na+)=
=0.1mol/L,
故选:B;
| 1×2×10 -3 |
| 2 |
由消耗1mol?L-1Na2SO4溶液1ml,发生反应为Ba2++SO42-═BaSO4↓,则Ba2+离子的物质的量为10-3mol;
由消耗1mol?L-1AgNO3溶液5ml,发生反应为Cl-+Ag+═AgCl↓,则Cl-离子的物质的量为5×10-3mol;
设每份中的钠离子的物质的量为x,混合溶液不显电性,
则x+10-3mol×2+10-3mol×2=5×10-3mol,x=10-3mol,则原溶液中的钠离子浓度为c(Na+)=
| 10 -3mol |
| 0.01L |
故选:B;
点评:本题考查学生利用离子反应方程式的计算,明确离子之间的量的关系即可解答,利用溶液不显电性来计算钠离子的物质的量是解答的关键,题目难度中等.

练习册系列答案
 名题训练系列答案
名题训练系列答案 期末集结号系列答案
期末集结号系列答案
相关题目
有2份质量分数不同的NaHCO3和NaOH的混合物,将它们分别用酒精灯加热至恒重测得的数据如下:经分析得到的15.600g固体是纯净物.则下列叙述正确的是( )
| 第1份 | 第2份 | |
| 混合物质量(g) | 9.2 | 18.4 |
| 反应后固体质量(g) | 8.3 | 15.6 |
| A、本次实验至少要进行6次称重 |
| B、第1份混合物中NaOH的质量分数更大 |
| C、根据表中数据不能计算出第1份混合物中NaHCO3的质量分数 |
| D、第2份混合物中NaOH的质量分数小于0.32 |
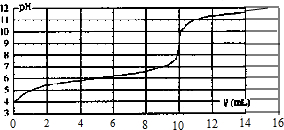 实验室用0.10mol?L-1的NaOH溶液滴定某一元弱酸HA的滴定曲线如图所示,图中横轴为滴入的NaOH溶液的体积V(mL),纵轴为溶液的pH,下列叙述不正确的是( )
实验室用0.10mol?L-1的NaOH溶液滴定某一元弱酸HA的滴定曲线如图所示,图中横轴为滴入的NaOH溶液的体积V(mL),纵轴为溶液的pH,下列叙述不正确的是( )| A、此一元弱酸HA的电离平衡常数Ka≈1×10-4mol?L-1 |
| B、此弱酸的起始浓度约为1×10-2mol?L-1 |
| C、此实验最好选用酚酞试液(变色范围8.0~10.0)做指示剂 |
| D、当混合液pH=7时,溶液中c(HA)>c(A-) |
在自来水蒸馏实验中,下列操作叙述不正确的是( )
A、在蒸馏烧瓶中盛约
| ||
| B、收集到的液体取少量滴入硝酸银和稀硝酸,无明显现象 | ||
| C、冷水从冷凝管下口进,上口出 | ||
| D、将温度计水银球插到蒸馏烧瓶内的自来水中 |
 金属钛(Ti)因其硬度大、熔点高、常温时耐酸碱腐蚀等性质被广泛用在高新科技材料和航天领域中.“硫酸法”生产钛的原料是钛铁矿(主要成分是:FeTiO3,还含有少量Mn、Zn、Cr、Cu等重金属元素及脉石等杂质);主要生产流程如图:
金属钛(Ti)因其硬度大、熔点高、常温时耐酸碱腐蚀等性质被广泛用在高新科技材料和航天领域中.“硫酸法”生产钛的原料是钛铁矿(主要成分是:FeTiO3,还含有少量Mn、Zn、Cr、Cu等重金属元素及脉石等杂质);主要生产流程如图: