题目内容
 金属钛(Ti)因其硬度大、熔点高、常温时耐酸碱腐蚀等性质被广泛用在高新科技材料和航天领域中.“硫酸法”生产钛的原料是钛铁矿(主要成分是:FeTiO3,还含有少量Mn、Zn、Cr、Cu等重金属元素及脉石等杂质);主要生产流程如图:
金属钛(Ti)因其硬度大、熔点高、常温时耐酸碱腐蚀等性质被广泛用在高新科技材料和航天领域中.“硫酸法”生产钛的原料是钛铁矿(主要成分是:FeTiO3,还含有少量Mn、Zn、Cr、Cu等重金属元素及脉石等杂质);主要生产流程如图:已知反应:
①将钛铁矿与浓H2SO4煮解:FeTiO3+2H2SO4(浓)
| ||
②加水热分解硫酸氧钛:TiOSO4+(n+1)H2O
| ||
请回答下列问题:
(1)副产品甲是
(2)上述生产流程中加入铁屑的目的是
(3)写出中间产品乙与焦炭、氯气在高温下发生反应的方程式为:
(4)“硫酸法”生产钛排放的废液对水体有哪些污染,请指出主要的两点:
①
针对其中一项污染,提出处理的方法:
考点:制备实验方案的设计,金属冶炼的一般原理
专题:几种重要的金属及其化合物
分析:由流程可知,钛铁矿(主要成分是:FeTiO3,还含有少量Mn、Zn、Cr、Cu等重金属元素及脉石等杂质)中加入浓硫酸,FeTiO3发生反应:FeTiO3+2H2SO4(浓)
TiOSO4(硫酸氧钛)+FeSO4+2H2O,钛铁矿和浓硫酸反应的产物之一是TiOSO4,加入铁屑,可防止Fe2+氧化,溶液Ⅰ中含有FeSO4和TiOSO4,溶液Ⅱ主要含有TiOSO4,加入水,加热可水解生成H2TiO3,经煅烧可生成TiO2,用氯气、碳反应可生成TiCl4,高温条件下与镁反应可生成Ti,
(1)根据流程可知副产品甲为FeSO4?7H2O,可循环利用的物质是硫酸;
(2)铁能够与铁离子反应,加入铁粉可防止铁离子氧化;
(3)乙为TiO2,反应物为乙为TiO2、氯气、C,反应产物为四氯化钛和CO,反应条件为高温,据此写出反应的化学方程式;
(4)“硫酸法”排放的废液为酸性,会产生酸污染;与Ti共存的其它重金属的废液对水体有污染,可以用熟石灰治理污染.
| ||
(1)根据流程可知副产品甲为FeSO4?7H2O,可循环利用的物质是硫酸;
(2)铁能够与铁离子反应,加入铁粉可防止铁离子氧化;
(3)乙为TiO2,反应物为乙为TiO2、氯气、C,反应产物为四氯化钛和CO,反应条件为高温,据此写出反应的化学方程式;
(4)“硫酸法”排放的废液为酸性,会产生酸污染;与Ti共存的其它重金属的废液对水体有污染,可以用熟石灰治理污染.
解答:
解:钛铁矿(主要成分是:FeTiO3,还含有少量Mn、Zn、Cr、Cu等重金属元素及脉石等杂质)中加入浓硫酸,FeTiO3发生反应:FeTiO3+2H2SO4(浓)
TiOSO4(硫酸氧钛)+FeSO4+2H2O,钛铁矿和浓硫酸反应的产物之一是TiOSO4,加入铁屑,可防止Fe2+氧化,溶液Ⅰ中含有FeSO4和TiOSO4,溶液Ⅱ主要含有TiOSO4,加入水,加热可水解生成H2TiO3,经煅烧可生成TiO2,用氯气、碳反应可生成TiCl4,高温条件下与镁反应可生成Ti,
(1)从流程图硫酸与过量的铁反应可知,副产品甲是FeSO4?7H2O,可循环利用的物质是硫酸,
故答案为:FeSO4?7H2O;硫酸;
(2)铁可与Fe3+反应生成Fe2+,加入铁屑,可防止Fe2+氧化,
故答案为:防止Fe2+氧化(成Fe3+);
(3)中间产物乙为TiO2,TiO2与焦炭、氯气在高温下发生反应生成四氯化钛和一氧化碳,反应的方程式为:TiO2+2Cl2+2C
TiCl4+2CO,
故答案为:TiO2+2Cl2+2C
TiCl4+2CO;
(4)①②“硫酸法”生产钛排放的废液为酸性,会产生酸污染,并且与Ti共存的其它重金属的废液对水体有污染,
故答案为:①酸污染 ②重金属离子(Cu2+、Cr3+等)污染;
针对产生酸污染可以加入熟石灰中和,针对重金属离子污染可通过沉淀法除去,
故答案为:沉淀法.
| ||
(1)从流程图硫酸与过量的铁反应可知,副产品甲是FeSO4?7H2O,可循环利用的物质是硫酸,
故答案为:FeSO4?7H2O;硫酸;
(2)铁可与Fe3+反应生成Fe2+,加入铁屑,可防止Fe2+氧化,
故答案为:防止Fe2+氧化(成Fe3+);
(3)中间产物乙为TiO2,TiO2与焦炭、氯气在高温下发生反应生成四氯化钛和一氧化碳,反应的方程式为:TiO2+2Cl2+2C
| ||
故答案为:TiO2+2Cl2+2C
| ||
(4)①②“硫酸法”生产钛排放的废液为酸性,会产生酸污染,并且与Ti共存的其它重金属的废液对水体有污染,
故答案为:①酸污染 ②重金属离子(Cu2+、Cr3+等)污染;
针对产生酸污染可以加入熟石灰中和,针对重金属离子污染可通过沉淀法除去,
故答案为:沉淀法.
点评:本题考查物质的制备实验方案的设计,题目难度中等,试题侧重于学生的分析能力和实验能力的考查,为高考常见题型,明确制备流程及反应原理为解答关键,注意把握实验的基本原理和常见物质的性质.

练习册系列答案
 快乐暑假暑假能力自测中西书局系列答案
快乐暑假暑假能力自测中西书局系列答案
相关题目
下列溶液中Cl-浓度最小的是( )
| A、100mL 0.5mol/L KClO3溶液 |
| B、200mL 2.5mol/L MgCl2溶液 |
| C、300mL 2mol/L AlCl3溶液 |
| D、400mL1mol/L 盐酸 |
将一定质量的镁、铝合金加入到一定浓度的硝酸中,两者恰好完全反应,假设反应过程中还原产物只有NO和NO2,将产生的气体用排水集气法收集.得到0.1mol气体.然后向所得溶液中加入NaOH溶液至金属离子恰好沉淀完全.则下列有关叙述中正确的是( )
| A、加入合金的质量可能为3.2g |
| B、参加反应的硝酸的物质的量为0.4mol |
| C、沉淀完全时消耗NaOH的物质的量为0.3mol |
| D、还原产物的体积范围2.24L<V还原产物<6.72L |
取三份由NaCl、MgCl2、BaCl2溶液组成的营养液各10ml,分别加入1mol?L-1的NaOH、Na2SO4、AgNO3溶液至恰好反应,消耗溶液的体积如图所示,该营养液中钠离子的浓度为( )
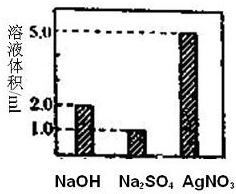

| A、0.5 mol?L-1 |
| B、0.1 mol?L-1 |
| C、1 mol?L-1 |
| D、1.5 mol?L-1 |
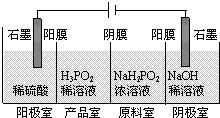
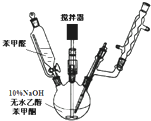 (1)制备过程中(如图),需在搅拌下滴加苯甲醛,并控制滴加速度使 反应温度维持在25~30℃,说明该反应是
(1)制备过程中(如图),需在搅拌下滴加苯甲醛,并控制滴加速度使 反应温度维持在25~30℃,说明该反应是