题目内容
7.在恒温恒容的密闭容器中进行的反应X(g)+3Y(g)?2Z(g),能够说明该反应达到平衡状态的是( )| A. | X、Y、Z的物质的量之比为1:3:2 | |
| B. | 容器内的压强不再随时间变化 | |
| C. | 单位时间内每消耗1molX,同时消耗3molY | |
| D. | 混合气体的密度不再随时间变化 |
分析 根据化学平衡状态的特征解答,当反应达到平衡状态时,正逆反应速率相等,各物质的浓度、百分含量不变,以及由此衍生的一些量也不发生变化,解题时要注意,选择判断的物理量,随着反应的进行发生变化,当该物理量由变化到定值时,说明可逆反应到达平衡状态.
解答 解:A、当体系达平衡状态时,X、Y、Z的物质的量之比为可能是1:3:2,也可能不是,与各物质的初始浓度及转化率有关,故A错误;
B、随着反应的进行体系压强逐渐减小,容器内压强保持不变说明达平衡状态,故B正确;
C、单位时间内每消耗1molX,同时消耗3molY,都体现正反应方向,故C错误;
D、混合气体的密度一直不随时间变化而变化,故D错误;
故选B.
点评 本题考查了化学平衡状态的判断,难度不大,注意当反应达到平衡状态时,正逆反应速率相等,但不为0.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
17.官能团决定了有机物主要的化学性性,下列有关描述正确的是( )
| A. | 醛基的结构简式为-COH | |
| B. | 乙烯和乙醇都能使溴水和酸性KMnO4溶液褪色 | |
| C. | 乙酸乙酯中的官能团为酯基(-COO-),能发生水解反应 | |
| D. | 苯能与氢气发生加成反应,是因为苯分子中含有碳碳双键 |
18.在合成氨反应中,将等物质的量的氮气和氢气充入一密闭容器中发生反应,测得 2min 内氨的平均反应速率为 2mol•L-1•min-1,2min 末 N2 的浓度为 7mol•L-1,则氢气的起始浓度为( )
| A. | 9mol•L-1 | B. | 6mol•L-1 | C. | 3mol•L-1 | D. | 2mol•L-1 |
12.常温下,pH=3的盐酸与pH=11的氨水等体积混合后的溶液,向该溶液中滴入2~3滴酚酞,溶液的颜色可能是( )
| A. | 只显红色 | B. | 呈无色 | C. | 无色或蓝色 | D. | 红色或无色 |
19.用层析法分离Fe3+和Cu2+的实验中,层析操作后,要将滤纸放在盛有浓氨水的试剂瓶口.为增强效果,可在浓氨水中加入( )
| A. | 氢氧化钠 | B. | 浓盐酸 | C. | 水 | D. | 硫酸铵 |
10.下列说法中正确的是( )
| A. | 决定化学反应速率的主要因素是反应物的浓度、压强、温度、催化剂等 | |
| B. | 测定HCl和NaOH反应的中和热时,每次实验均应测量3个温度,即盐酸的起始温度.NaOH溶液的起始温度和反应后反应体系的最高温度 | |
| C. | 稀醋酸与稀NaOH溶液反应生成1mol水,放出57.3kJ热量 | |
| D. | 某可逆反应的化学平衡常数K,只随温度的改变而改变,且温度越高K值一定越大 |
11.向某密闭容器中充入1mol CO和2mol H2O(g),发生反应:CO+H2O(g)?CO2+H2 ;△H<0.当反应达到平衡时,CO的体积分数为x.若维持容器的体积和温度不变,超始物质按下列四种情况充入该容器中,达到平衡时CO的体积分数大于x的是( )
| A. | 0.5mol CO+2mol H2O(g)+1mol CO2+1mol H2 | |
| B. | 1 mol CO+1mol H2O(g)+1mol CO2+1mol H2 | |
| C. | 0.5mol CO+1.5mol H2O(g)+0.4mol CO2+0.4mol H2 | |
| D. | 0.5mol CO+1.5mol H2O(g)+0.5mol CO2+0.5mol H2 |
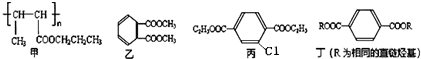
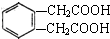 ;
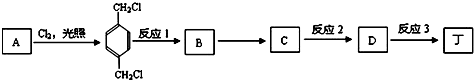
;
 .
.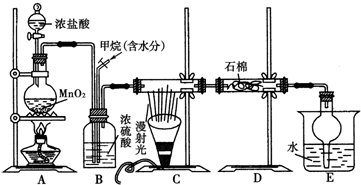 利用甲烷和氯气发生取代反应制取副产品盐酸的设想在工业上已成为现实.某化学兴趣小组通过在实验室中模拟上述过程,其设计的模拟装置如图所示,根据要求填空:
利用甲烷和氯气发生取代反应制取副产品盐酸的设想在工业上已成为现实.某化学兴趣小组通过在实验室中模拟上述过程,其设计的模拟装置如图所示,根据要求填空: