题目内容
17.官能团决定了有机物主要的化学性性,下列有关描述正确的是( )| A. | 醛基的结构简式为-COH | |
| B. | 乙烯和乙醇都能使溴水和酸性KMnO4溶液褪色 | |
| C. | 乙酸乙酯中的官能团为酯基(-COO-),能发生水解反应 | |
| D. | 苯能与氢气发生加成反应,是因为苯分子中含有碳碳双键 |
分析 A.醛基的结构简式为-CHO;
B.乙醇和溴水不反应;
C.乙酸乙酯含有酯基,可发生水解反应;
D.苯不含碳碳双键.
解答 解:A.醛基的结构简式为-CHO,故A错误;
B.乙烯含有碳碳双键,可与溴水发生加成反应,但乙醇和溴水不反应,故B错误;
C.乙酸乙酯含有酯基,为-COO-,为酯化反应的逆反应,可发生水解反应生成酸和醇,故C正确;
D.苯可发生加成反应,但不含碳碳双键,故D错误.
故选C.
点评 本题考查有机物的结构和性质,为高频考点,侧重于学生的分析能力的考查,注意把握有机物的结构和官能团的性质,难度不大.

练习册系列答案
相关题目
7.部分弱酸的电离平衡常数如表:
在25℃时,下列选项不正确的是( )
| 弱酸 | HCOOH | HCN | H2CO3 |
| 电离常数(25℃) | Ka=1.77×10-4 | Ka=4.9×10-10 | Ka1=4.3×10-7 Ka2=5.6×10-11 |
| A. | 反应CN-+H2O+CO2═HCN+HCO3-能够发生 | |
| B. | 中和等体积、等pH的HCOOH和HCN消耗NaOH的量,前者小于后者 | |
| C. | 物质的量浓度相等的HCOONa和KCN溶液中,c(Na+)-{c(HCOO-)}<c(K+)-c(CN-) | |
| D. | c(NH4+)相等的HCOONH4溶液、NH4CN溶液、NH4HCO3溶液中,c(NH4HCO3)>c(NH4CN)>c(HCOONH4) |
12.下列反应既属于氧化还原反应,又是吸热反应的是( )
| A. | 锌粒与稀硫酸的反应 | |
| B. | 甲烷在空气中燃烧的反应 | |
| C. | 灼热的木炭与CO2的反应 | |
| D. | Ba(OH)2•8H2O晶体与NH4Cl晶体的反应 |
2.某物质的产量能用来衡量一个国家石油化工发展水平,该物质是( )
| A. | 苯 | B. | 甲烷 | C. | 乙烯 | D. | 乙醇 |
9.关于下列实验的叙述正确的是( )
| A. | 实验室制备氯气是利用了二氧化锰的还原性 | |
| B. | 实验室制备氯气时使用过量的浓盐酸可使二氧化锰完全反应 | |
| C. | 用金属与氯气直接化合或金属与盐酸反应都可制得FeCl2 | |
| D. | 将Cl2与HCl混合气体通过四氯化碳可得到纯净的Cl2 |
6.下列离子方程式书写正确的是( )
| A. | 将少量SO2气体这入NaClO溶液中:SO2+2ClO-+H2O═SO32-+2HCLO | |
| B. | 向KHSO4溶液中加入Ba(OH)2溶液的pH=7:Ba2++OH-+H++SO42-═BaSO4↓+H2O | |
| C. | 向Ca(H2PO4)2溶液中滴入过量的NaOH溶液:3Ca2++6H2PO4-+12OH-═Ca3(PO4)2↓+12H2O+$4PO_{4}^{-}}$ | |
| D. | 112mL(S.T.P)Cl2通入10ml1mol/L的FeBr2溶液:2Fe2++4Br-+3CL2═2Fe3++6Cl-+2Br2 |
7.在恒温恒容的密闭容器中进行的反应X(g)+3Y(g)?2Z(g),能够说明该反应达到平衡状态的是( )
| A. | X、Y、Z的物质的量之比为1:3:2 | |
| B. | 容器内的压强不再随时间变化 | |
| C. | 单位时间内每消耗1molX,同时消耗3molY | |
| D. | 混合气体的密度不再随时间变化 |
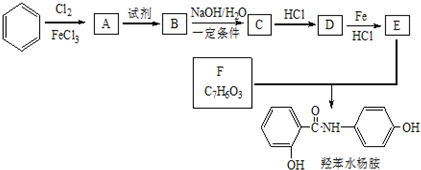
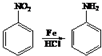
 +2NaOH$→_{一定条件}^{水}$
+2NaOH$→_{一定条件}^{水}$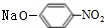 +NaCl+H2O.
+NaCl+H2O.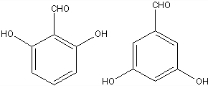 、
、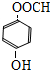 (任意一种).
(任意一种). 利用如图装置还可以验证醋酸、苯酚、碳酸的酸性强弱.
利用如图装置还可以验证醋酸、苯酚、碳酸的酸性强弱.