题目内容
12.常温下,pH=3的盐酸与pH=11的氨水等体积混合后的溶液,向该溶液中滴入2~3滴酚酞,溶液的颜色可能是( )| A. | 只显红色 | B. | 呈无色 | C. | 无色或蓝色 | D. | 红色或无色 |
分析 根据两种溶液中H+和OH-的关系以及氨水为弱电解质的性质,判断反应后酸碱的过量,进而判断反应后溶液的酸碱性,结合酚酞的变色范围为8-10解答该题.
解答 解:pH=3的盐酸中c(H+)=10-3mol/L,pH=11的氨水中c(OH-)=10-3mol/L,两种溶液H+与OH-离子浓度相等,但由于氨水为弱电解质,不能完全电离,则氨水浓度大于盐酸浓度,反应后氨水过量,溶液呈碱性,则所得溶液的pH>7,滴加酚酞,如pH<8,则呈无色,如pH>8,则呈红色,
故选D.
点评 本题考查酸碱混合溶液定性判断,为高频考点,侧重于学生的分析能力的考查,明确混合溶液中的溶质及其性质是解本题关键,注意把握酚酞的变色范围,题目难度不大.

练习册系列答案
相关题目
2.某物质的产量能用来衡量一个国家石油化工发展水平,该物质是( )
| A. | 苯 | B. | 甲烷 | C. | 乙烯 | D. | 乙醇 |
3.目前世界上 60%的镁是从海水中提取的.学生就这个课题展开了讨论.已知海水提镁的主要步骤如图:
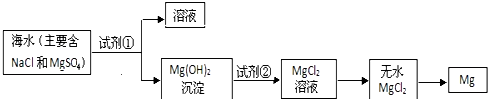
(一)在海水提镁的过程中如何实现对镁离子的富集?学生提出三个不同观点.
观点 1:直接往海水中加入沉淀剂.
观点 2:高温加热蒸发海水后,再加入沉淀剂.
观点 3:利用晒盐后的苦卤水,再加入沉淀剂.
请你评价三个学生提出的观点是否正确(填是或否),并简述理由.
(二)在海水提镁的过程中如何实现对镁离子的分离?
(1)为了使镁离子沉淀下来,加入的足量试剂①是Ca(OH)2(填化学式).
(2)加入的足量试剂②是HCl(填化学式).
(3)试从节约能源,提高金属镁的纯度分析,以下适宜的冶镁方法是c.
a.Mg(OH)2$\stackrel{△}{→}$MgO$→_{2800℃}^{电解}$Mg b.Mg(OH)2$\stackrel{△}{→}$MgO$\stackrel{C}{→}$Mg
c.Mg(OH)2$\stackrel{HCl}{→}$MgCl2$→_{714℃}^{电解}$Mg d.Mg(OH)2$\stackrel{HCl}{→}$MgCl2$→_{还原}^{活泼金属}$Mg.

(一)在海水提镁的过程中如何实现对镁离子的富集?学生提出三个不同观点.
观点 1:直接往海水中加入沉淀剂.
观点 2:高温加热蒸发海水后,再加入沉淀剂.
观点 3:利用晒盐后的苦卤水,再加入沉淀剂.
请你评价三个学生提出的观点是否正确(填是或否),并简述理由.
| 学生观点 | 是否正确 | 简述理由 |
| 观点 1 | 否 | 海水中镁离子浓度小,沉淀剂的用量大,不利于镁离子的沉淀 |
| 观点 2 | 否 | 能源消耗大,海水的综合利用低,成本高 |
| 观点 3 | 是 | 镁离子富集浓度高,成本低 |
(1)为了使镁离子沉淀下来,加入的足量试剂①是Ca(OH)2(填化学式).
(2)加入的足量试剂②是HCl(填化学式).
(3)试从节约能源,提高金属镁的纯度分析,以下适宜的冶镁方法是c.
a.Mg(OH)2$\stackrel{△}{→}$MgO$→_{2800℃}^{电解}$Mg b.Mg(OH)2$\stackrel{△}{→}$MgO$\stackrel{C}{→}$Mg
c.Mg(OH)2$\stackrel{HCl}{→}$MgCl2$→_{714℃}^{电解}$Mg d.Mg(OH)2$\stackrel{HCl}{→}$MgCl2$→_{还原}^{活泼金属}$Mg.
7.在恒温恒容的密闭容器中进行的反应X(g)+3Y(g)?2Z(g),能够说明该反应达到平衡状态的是( )
| A. | X、Y、Z的物质的量之比为1:3:2 | |
| B. | 容器内的压强不再随时间变化 | |
| C. | 单位时间内每消耗1molX,同时消耗3molY | |
| D. | 混合气体的密度不再随时间变化 |
17.用CO合成甲醇的热化学方程式为CO(g)+2H2(g)?CH3OH(g)△H<0.下列不能说明反应已达平衡状态的是( )
| A. | 单位时间内生成2mol H2的同时消耗了1mol CO | |
| B. | c(CO):c(CH3OH)=1:1 | |
| C. | 在恒温恒容的容器中,混合气体的压强保持不变 | |
| D. | 在绝热恒容的容器中,反应的平衡常数不再变化 |
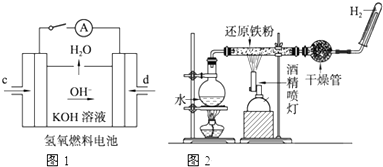
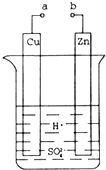 原电池是化学对人类的一项重大贡献.某兴趣小组为研究原电池原理,设计如图装置.
原电池是化学对人类的一项重大贡献.某兴趣小组为研究原电池原理,设计如图装置.