题目内容
18.在合成氨反应中,将等物质的量的氮气和氢气充入一密闭容器中发生反应,测得 2min 内氨的平均反应速率为 2mol•L-1•min-1,2min 末 N2 的浓度为 7mol•L-1,则氢气的起始浓度为( )| A. | 9mol•L-1 | B. | 6mol•L-1 | C. | 3mol•L-1 | D. | 2mol•L-1 |
分析 在合成氨反应中,将等物质的量的氮气和氢气充入一密闭容器中发生反应,测得 2min 内氨的平均反应速率为 2mol•L-1•min-1,则上层氨气的浓度=2mol•L-1•min-1×2min=4mol/L,2min 末 N2 的浓度为 7mol•L-1,结合化学平衡三行计算计算,起始量-变化量=某时刻量列式计算得到.
解答 解:将等物质的量的氮气和氢气充入一密闭容器中发生反应,测得 2min 内氨的平均反应速率为 2mol•L-1•min-1,则上层氨气的浓度=2mol•L-1•min-1×2min=4mol/L,则消耗氮气浓度为2mol/L,消耗氢气浓度为6mol/L,2min 末 N2 的浓度为 7mol•L-1,则氮气起始量浓度为9mol/L,列式得到
N2+3H2=2NH3
起始量(mol/L) 9 9 0
变化量(mol/L) 2 6 4
2min量(mol/L) 7 3 4
氢气的起始浓度9mol/L,
故选A.
点评 本题考查了化学反应速率、化学三行计算的理解应用,掌握基础是解题关键,题目难度不大.

练习册系列答案
相关题目
9.关于下列实验的叙述正确的是( )
| A. | 实验室制备氯气是利用了二氧化锰的还原性 | |
| B. | 实验室制备氯气时使用过量的浓盐酸可使二氧化锰完全反应 | |
| C. | 用金属与氯气直接化合或金属与盐酸反应都可制得FeCl2 | |
| D. | 将Cl2与HCl混合气体通过四氯化碳可得到纯净的Cl2 |
6.下列离子方程式书写正确的是( )
| A. | 将少量SO2气体这入NaClO溶液中:SO2+2ClO-+H2O═SO32-+2HCLO | |
| B. | 向KHSO4溶液中加入Ba(OH)2溶液的pH=7:Ba2++OH-+H++SO42-═BaSO4↓+H2O | |
| C. | 向Ca(H2PO4)2溶液中滴入过量的NaOH溶液:3Ca2++6H2PO4-+12OH-═Ca3(PO4)2↓+12H2O+$4PO_{4}^{-}}$ | |
| D. | 112mL(S.T.P)Cl2通入10ml1mol/L的FeBr2溶液:2Fe2++4Br-+3CL2═2Fe3++6Cl-+2Br2 |
13.2002 年,科学家获得了 6 个非常罕见的 Fe-45 原子,这 6 个原子中发生了双质子衰变,既由一个原子核同时放出两个质子的衰变方式,以下有关原子${\;}_{26}^{45}$Fe的说法正确的是( )
| A. | 该原子中子数与质子数之差为 19 | |
| B. | 他们获得了一种新元素 | |
| C. | ${\;}_{26}^{45}$Fe与${\;}_{26}^{56}$Fe的化学性质几乎完全相同 | |
| D. | 这种铁原子衰变出 2 个质子后变成${\;}_{26}^{43}$Fe |
3.目前世界上 60%的镁是从海水中提取的.学生就这个课题展开了讨论.已知海水提镁的主要步骤如图:
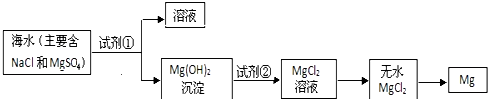
(一)在海水提镁的过程中如何实现对镁离子的富集?学生提出三个不同观点.
观点 1:直接往海水中加入沉淀剂.
观点 2:高温加热蒸发海水后,再加入沉淀剂.
观点 3:利用晒盐后的苦卤水,再加入沉淀剂.
请你评价三个学生提出的观点是否正确(填是或否),并简述理由.
(二)在海水提镁的过程中如何实现对镁离子的分离?
(1)为了使镁离子沉淀下来,加入的足量试剂①是Ca(OH)2(填化学式).
(2)加入的足量试剂②是HCl(填化学式).
(3)试从节约能源,提高金属镁的纯度分析,以下适宜的冶镁方法是c.
a.Mg(OH)2$\stackrel{△}{→}$MgO$→_{2800℃}^{电解}$Mg b.Mg(OH)2$\stackrel{△}{→}$MgO$\stackrel{C}{→}$Mg
c.Mg(OH)2$\stackrel{HCl}{→}$MgCl2$→_{714℃}^{电解}$Mg d.Mg(OH)2$\stackrel{HCl}{→}$MgCl2$→_{还原}^{活泼金属}$Mg.

(一)在海水提镁的过程中如何实现对镁离子的富集?学生提出三个不同观点.
观点 1:直接往海水中加入沉淀剂.
观点 2:高温加热蒸发海水后,再加入沉淀剂.
观点 3:利用晒盐后的苦卤水,再加入沉淀剂.
请你评价三个学生提出的观点是否正确(填是或否),并简述理由.
| 学生观点 | 是否正确 | 简述理由 |
| 观点 1 | 否 | 海水中镁离子浓度小,沉淀剂的用量大,不利于镁离子的沉淀 |
| 观点 2 | 否 | 能源消耗大,海水的综合利用低,成本高 |
| 观点 3 | 是 | 镁离子富集浓度高,成本低 |
(1)为了使镁离子沉淀下来,加入的足量试剂①是Ca(OH)2(填化学式).
(2)加入的足量试剂②是HCl(填化学式).
(3)试从节约能源,提高金属镁的纯度分析,以下适宜的冶镁方法是c.
a.Mg(OH)2$\stackrel{△}{→}$MgO$→_{2800℃}^{电解}$Mg b.Mg(OH)2$\stackrel{△}{→}$MgO$\stackrel{C}{→}$Mg
c.Mg(OH)2$\stackrel{HCl}{→}$MgCl2$→_{714℃}^{电解}$Mg d.Mg(OH)2$\stackrel{HCl}{→}$MgCl2$→_{还原}^{活泼金属}$Mg.
10.工业上用洗净的废铜屑作原料来制备硝酸铜.下列设计路线符合“绿色化学”思想的是( )
| A. | Cu+HNO3(浓)→Cu(NO3)2 | B. | Cu+HNO3(稀)→Cu(NO3)2 | ||
| C. | Cu $\stackrel{空气}{→}$CuO$\stackrel{HNO_{3}}{→}$ Cu(NO3)2 | D. | Cu$\stackrel{浓硫酸}{→}$CuSO4$\stackrel{Ba(NO_{3})_{2}}{→}$Cu(NO3)2 |
7.在恒温恒容的密闭容器中进行的反应X(g)+3Y(g)?2Z(g),能够说明该反应达到平衡状态的是( )
| A. | X、Y、Z的物质的量之比为1:3:2 | |
| B. | 容器内的压强不再随时间变化 | |
| C. | 单位时间内每消耗1molX,同时消耗3molY | |
| D. | 混合气体的密度不再随时间变化 |
2.下列属于多糖的是( )
| A. | 葡萄糖 | B. | 蔗糖 | C. | 淀粉 | D. | CH3COOH |
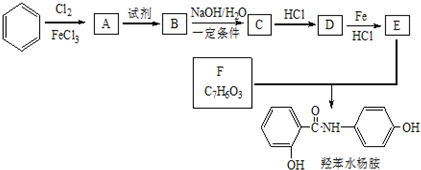
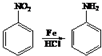
 +2NaOH$→_{一定条件}^{水}$
+2NaOH$→_{一定条件}^{水}$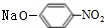 +NaCl+H2O.
+NaCl+H2O.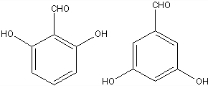 、
、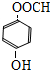 (任意一种).
(任意一种).