题目内容
6.下列生活生产中常见物质的化学式与名称相对应的是( )| A. | FeS04•7H20-绿矾 | B. | Na2O2-火碱 | C. | BaC03-重晶石 | D. | C6Hl206-庶糖 |
分析 A.FeS04•7H20俗称绿矾;
B.氢氧化钠俗称火碱、烧碱、苛性钠;
C.重晶石是钡的最常见矿物,它的成分为硫酸钡;
D.C6Hl206存在同分异构现象.
解答 解:A.七水硫酸亚铁,俗称绿矾,化学式为FeS04•7H20,故A正确;
B.氢氧化钠俗称火碱、烧碱、苛性钠,化学式为NaOH,故B错误;
C.重晶石是钡的最常见矿物,它的成分为硫酸钡,化学式为BaSO4,故C错误;
D.C6Hl206存在同分异构现象,可能是葡萄糖也可能是果糖,故D错误;
故选A.
点评 本题考查了常见物质的俗名与化学式的判断,题目难度不大,试题侧重了基础知识的考查,注意熟练掌握物质的化学式与俗名的关系.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
2.一定量的Cu和1mol•L-1 的稀硝酸反应,如果NO3-的浓度下降0.2mol•L-1,则溶液中c(H+)同时下降(假定反应前后溶液体积不变)( )
| A. | 0.8mol•L-1 | B. | 0.6mol•L-1 | C. | 0.4mol•L-1 | D. | 0.2mol•L-1 |
3.以下相关物质的信息都正确的一项是( )
| 选项 | 化学式 | 电子式或含有的化学键类型 | 物质的性质 | 与性质相对应的用途 |
| A | NaClO | 离子键 共价键 | 强氧化性 | 消毒剂 |
| B | H2O2 | 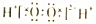 | 不稳定,易分解 | 医用消毒剂 |
| C | NH3 | 共价键 | 水溶液呈弱碱性 | 工业制硝酸 |
| D | NaHCO3 | 离子键 | 受热易分解 | 泡沫灭火器 |
| A. | A | B. | B | C. | C | D. | D |
14.某化学小组用粗氧化铜(含少量氧化亚铁及不溶于酸的杂质)制取氯化铜,其实验流程如下所示:
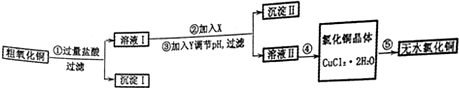
已知:
提供的试剂:A.NaOH B.H2O2 C.Na2CO3 D.CuO
(1)步骤②反应的离子方程式是2Fe2++H2O2+2H+=2Fe3++2H2O.步骤③中调节溶液pH的范围是3.2~4.7之间.
(2)如何判断沉淀Ⅱ已洗涤干净的方法是取最后一次洗涤液,加入硝酸酸化,再滴入硝酸银溶液,没有白色沉淀生成,说明洗涤干净,否则洗涤不干净.
(3)步骤④的方法是加热浓缩、冷却结晶、过滤、洗涤,
(4)步骤⑤要得到无水氯化铜,需要在赶在的HCl气流中加热CuCl2•2H2O其原因是干燥的HCl气流既可抑制Cu2+的水解,还能带走CuCl2•2H2O受热产生的水汽.
(5)若用电解法精炼铜,则阴极的电极反应式为Cu2++2e-=Cu.

已知:
| 金属离子 | 氢氧化物开始沉淀时的pH | 氢氧化物沉淀完全时的pH |
| Fe3+ | 1.9 | 3.2 |
| Fe2+ | 7.0 | 9.0 |
| Cu2+ | 4.7 | 6.7 |
(1)步骤②反应的离子方程式是2Fe2++H2O2+2H+=2Fe3++2H2O.步骤③中调节溶液pH的范围是3.2~4.7之间.
(2)如何判断沉淀Ⅱ已洗涤干净的方法是取最后一次洗涤液,加入硝酸酸化,再滴入硝酸银溶液,没有白色沉淀生成,说明洗涤干净,否则洗涤不干净.
(3)步骤④的方法是加热浓缩、冷却结晶、过滤、洗涤,
(4)步骤⑤要得到无水氯化铜,需要在赶在的HCl气流中加热CuCl2•2H2O其原因是干燥的HCl气流既可抑制Cu2+的水解,还能带走CuCl2•2H2O受热产生的水汽.
(5)若用电解法精炼铜,则阴极的电极反应式为Cu2++2e-=Cu.
1.50℃时,下列各溶液中,离子的物质的量浓度关系正确的是( )
| A. | 饱和食盐水中:c(Na+)+c(H+)=c(Cl-)+c(OH-) | |
| B. | 饱和小苏打溶液中:c(Na+)=c(HCO3-) | |
| C. | pH=4的醋酸中:c(H+)=4.0mol•L-1 | |
| D. | pH=12的纯碱溶液中:c(OH-)=1.0×10-2mol•L-1 |
16.一氧化碳还原氧化铁:Fe2O3+3CO$\frac{\underline{\;\;△\;\;}}{\;}$2Fe+3CO2,在该反应中( )
| A. | 铁做还原剂 | B. | Fe2O3做氧化剂 | ||
| C. | 铁元素被还原 | D. | 铁元素化合价升高 |

 汽车安全气囊一般由传感器、气囊、气体发生器等组成.
汽车安全气囊一般由传感器、气囊、气体发生器等组成.