题目内容
3.以下相关物质的信息都正确的一项是( )| 选项 | 化学式 | 电子式或含有的化学键类型 | 物质的性质 | 与性质相对应的用途 |
| A | NaClO | 离子键 共价键 | 强氧化性 | 消毒剂 |
| B | H2O2 | 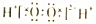 | 不稳定,易分解 | 医用消毒剂 |
| C | NH3 | 共价键 | 水溶液呈弱碱性 | 工业制硝酸 |
| D | NaHCO3 | 离子键 | 受热易分解 | 泡沫灭火器 |
| A. | A | B. | B | C. | C | D. | D |
分析 A.NaClO中含有离子键和共价键,具有强氧化性,能使蛋白质变性;
B.过氧化氢中只含共价键,为共价化合物,但不稳定,易分解生成水和氧气,具有强氧化性;
C.氨气中只含共价键,氨气溶于水生成一水合氨而使其溶液呈碱性,氨气能被催化氧化生成NO而制取硝酸;
D.NaHCO3中含有离子键和共价键,但性质不稳定,受热易分解生成二氧化碳,能和硫酸铝发生双水解反应而生成二氧化碳.
解答 解:A.NaClO中钠离子和次氯酸根离子之间存在离子键、Cl-O原子之间存在共价键,次氯酸钠具有强氧化性,能使蛋白质变性而作消毒剂,故A正确;
B.双氧水中H-O、O-O原子之间只存在共价键,为共价化合物,电子式为 ,故B错误;
,故B错误;
C.氨气中N-H原子之间只含共价键,氨气溶于水生成一水合氨,NH3.H2O电离出OH-而使其溶液呈碱性,氨气能被催化氧化生成NO而制取硝酸,但与氨气水溶液呈碱性无关,故C错误;
D.NaHCO3中含有离子键和共价键,但性质不稳定,受热易分解生成二氧化碳,能和硫酸铝发生双水解反应而生成二氧化碳,与 NaHCO3的不稳定性无关,故D错误;
故选A.
点评 本题考查化学用语、物质的性质和用途,为高频考点,明确物质中存在的化学键、物质的性质与用途关系是解本题关键,性质决定用途,用途体现性质,题目难度不大.

练习册系列答案
 导学教程高中新课标系列答案
导学教程高中新课标系列答案
相关题目
13.某研究性学习小组对钠在CO2气体中燃烧进行了下列实验:
(1)该小组同学对管壁的白色物质的成分进行讨论并提出假设:
Ⅰ.白色物质可能是Na2O;
Ⅱ.白色物质可能是Na2CO3
Ⅲ.白色物质还可能是Na2O和Na2CO3混合物
(2)为确定该白色物质的成分,该小组进行了如下实验:
①通过对上述实验的分析,你认为上述三个假设中,Ⅱ成立.
②则钠在CO2中燃烧的化学方程式为4Na+3CO2$\frac{\underline{\;点燃\;}}{\;}$2Na2CO3+C.
③丙同学认为白色物质有可能是氢氧化钠,你认为是否合理并说出理由不正确,因为反应物中无H元素(或违背质量守恒定律).
(3)丁同学称取Na2O样品mg(假设只含有Na2O2杂质),请你与他合作从下面选用合适的仪器和试剂,设计一种可选用的实验仪器组合,填写下表以完成样品中Na2O含量的测定.可选用的试剂:
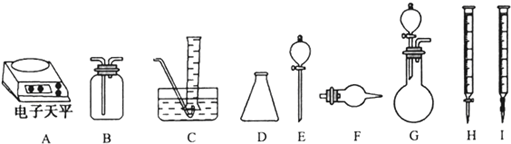
a.浓硫酸 b.水 c.盐酸标准溶液 d.NaOH 标准溶液 e.酚酞 f.碱石灰 g.稀盐酸
(4)某学生设计了以下实验方案来测定该试样中Na2O的质量分数,其操作流程和实验数据如下:
7.75gNa2O样品$\stackrel{在氧气中充分灼烧}{→}$固体$\stackrel{冷却}{→}$称量得固体9.35g.该Na2O产品中Na2O的质量分数为80%.
| 操作过程 | 实验现象 |
| 将干燥纯净的CO2缓缓通过放有钠的已排尽空气的干燥玻璃管中,加热 | 钠燃烧,火焰为黄色 |
| 反应后冷却 | 管壁附有黑色颗粒和白色物质 |
Ⅰ.白色物质可能是Na2O;
Ⅱ.白色物质可能是Na2CO3
Ⅲ.白色物质还可能是Na2O和Na2CO3混合物
(2)为确定该白色物质的成分,该小组进行了如下实验:
| 实验步骤 | 实验现象 |
| ①少量白色物质于试管中,加入适量水,振荡,样品全部溶于水,向其中加过量的CaC12溶液出现白色沉淀 | 出现白色沉淀 |
| ②静置片刻,取上层清液于试管中,滴加无色酚酞试液 | 无明显现象 |
②则钠在CO2中燃烧的化学方程式为4Na+3CO2$\frac{\underline{\;点燃\;}}{\;}$2Na2CO3+C.
③丙同学认为白色物质有可能是氢氧化钠,你认为是否合理并说出理由不正确,因为反应物中无H元素(或违背质量守恒定律).
(3)丁同学称取Na2O样品mg(假设只含有Na2O2杂质),请你与他合作从下面选用合适的仪器和试剂,设计一种可选用的实验仪器组合,填写下表以完成样品中Na2O含量的测定.可选用的试剂:

a.浓硫酸 b.水 c.盐酸标准溶液 d.NaOH 标准溶液 e.酚酞 f.碱石灰 g.稀盐酸
| 实验过程中发生反应的化学方程式 | 实验所需仪器(用字母表示) | 实验所需试剂(用字表示) | 实验需直接测定的有关物理量(用文字说明) |
7.75gNa2O样品$\stackrel{在氧气中充分灼烧}{→}$固体$\stackrel{冷却}{→}$称量得固体9.35g.该Na2O产品中Na2O的质量分数为80%.
14.下列有关化学实验安全问题的叙述中不正确的是( )
| A. | 浓硫酸沾到皮肤上时,可立刻用大量的水冲洗,然后再涂上3%~5%的NaHCO3溶液 | |
| B. | 取用化学药品时,应特别注意观察药品包装容器上的安全警示标志 | |
| C. | 凡是给玻璃仪器加热,都要加垫石棉网,以防仪器炸裂 | |
| D. | 闻任何化学药品的气味都不能将鼻子凑近药品 |
18.某有机物分子式为C3H4,仅从碳原子的连接形式和价键(单键、双键、三键)来讨论.其同分异构体有( )
| A. | 5种 | B. | 4种 | C. | 3种 | D. | 2种 |
2.关于下列反应,说法正确的是:(图中共有三种原子)( )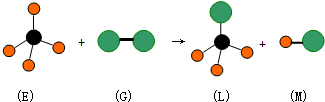

| A. | 反应过程中E中共价键断裂,G中共价键保持不动 | |
| B. | E中存在非极性键 | |
| C. | M分子有可能是HCl | |
| D. | 上述反应的类型是加成反应 |
6.下列生活生产中常见物质的化学式与名称相对应的是( )
| A. | FeS04•7H20-绿矾 | B. | Na2O2-火碱 | C. | BaC03-重晶石 | D. | C6Hl206-庶糖 |
7.下列关于浓硫酸的说法中,不正确的是( )
| A. | 常作为气体的干燥剂 | B. | 常温下不能与铁发生反应 | ||
| C. | 滴在蔗糖上,蔗糖会变黑 | D. | 工业上主要采用接触法制备 |
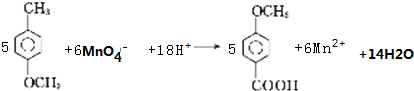 .
.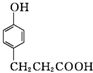 .
.