题目内容
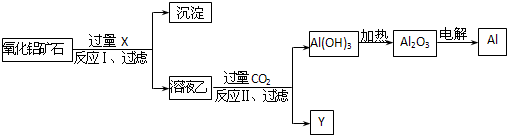
工业上用某种氧化铝矿石(含Fe2O3杂质)为原料冶炼铝的工艺流程如图:对上述流程中的判断正确的是( )

| A、试剂X可以为氨水,沉淀中含有铁的化合物 |
| B、CO2可以用H2SO4溶液或稀盐酸代替 |
| C、反应II中的反应为:CO2+AlO2-+2H2O=Al(OH)3↓+HCO3- |
| D、工业上还可采用Fe还原Al2O3的方法制Al,成本更低 |
考点:物质分离和提纯的方法和基本操作综合应用
专题:实验设计题
分析:综合分析工艺流程图可知,试剂X是氢氧化钠溶液,Al2O3溶于氢氧化钠溶液得到NaAlO2溶液,Fe2O3与氢氧化钠溶液不反应,所以反应Ⅰ过滤后所得溶液乙为NaAlO2溶液,沉淀为Fe2O3;向NaAlO2溶液中通入过量CO2的化学方程式为NaAlO2+CO2+2H2O=Al(OH)3↓+NaHCO3,溶液Y为NaHCO3,Al(OH)3加热分解生成Al2O3,电解熔融Al2O3生成Al,以此解答该题.
解答:
解:综合分析工艺流程图可知,试剂X是氢氧化钠溶液,Al2O3溶于氢氧化钠溶液得到NaAlO2溶液,Fe2O3与氢氧化钠溶液不反应,所以反应Ⅰ过滤后所得溶液乙为NaAlO2溶液,沉淀为Fe2O3;向NaAlO2溶液中通入过量CO2的化学方程式为NaAlO2+CO2+2H2O=Al(OH)3↓+NaHCO3,溶液Y为NaHCO3,Al(OH)3加热分解生成Al2O3,电解熔融Al2O3生成Al,
A.分离氧化铝和氧化铁,只能用氢氧化钠溶液,不能用氨水,因氧化铝与氨水不反应,故A错误;
B.CO2可以和偏铝酸钠反应制得氢氧化铝,用H2SO4溶液或稀盐酸代替会导致生成的氢氧化铝溶于其中,故B错误;
C.过量的二氧化碳与偏铝酸钠反应生成氢氧化铝沉淀与碳酸氢钠,反应方程式为NaAlO2+CO2+2H2O=Al(OH)3↓+NaHCO3,即CO2+AlO2-+2H2O═Al(OH)3↓+HCO3-,故C正确;
D.Fe活泼性较Al弱,与Al2O3不反应,故D错误.
故选C.
A.分离氧化铝和氧化铁,只能用氢氧化钠溶液,不能用氨水,因氧化铝与氨水不反应,故A错误;
B.CO2可以和偏铝酸钠反应制得氢氧化铝,用H2SO4溶液或稀盐酸代替会导致生成的氢氧化铝溶于其中,故B错误;
C.过量的二氧化碳与偏铝酸钠反应生成氢氧化铝沉淀与碳酸氢钠,反应方程式为NaAlO2+CO2+2H2O=Al(OH)3↓+NaHCO3,即CO2+AlO2-+2H2O═Al(OH)3↓+HCO3-,故C正确;
D.Fe活泼性较Al弱,与Al2O3不反应,故D错误.
故选C.
点评:本题以铁、铝化合物的性质为载体综合考查工业冶炼铝等知识,侧重于考查学生分析和解决问题的能力,综合性强,为高考常见题型,注意把握制备原理和反应的流程,难度中等.

练习册系列答案
相关题目
在解释下列物质性质的变化规律与物质结构间的因果关系时,与化学键的强弱无关的变化规律是( )
| A、HF、HCl、HBr、HI的热稳定依次减弱 |
| B、金刚石的硬度大于硅,其熔、沸点也高于硅 |
| C、NaF、NaCl、NaBr、NaI的熔点依次减小 |
| D、F2、Cl2、Br2、I2的熔、沸点逐渐升高 |
PCl3和PCl5都是重要的化工原料.将PCl3(g) 和Cl2(g)充入体积不变的2 L密闭容器中,在一定条件下发生下述反应,并于10 min时达到平衡:PCl3(g)+Cl3(g)?PCl3(g).有关数据如下:
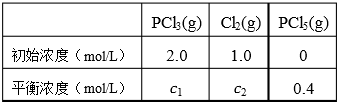
下列判断不正确的是( )

下列判断不正确的是( )
| A、10 min内,v(Cl2)=0.04 mol/(L?min) |
| B、当容器中Cl2为1.2 mol时,反应达到平衡 |
| C、升高温度(T1<T2),反应的平衡常数减小,平衡时PCl3的转化率变大 |
| D、平衡后移走2.0 mol PCl3和1.0 molCl2,在相同条件下再达平衡时,c(PCl5)<0.2 mol/L |
下列能达到实验目的是( )
A、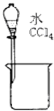 分离水和CCl4 |
B、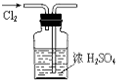 干燥Cl2 |
C、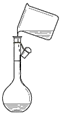 转移溶液 |
D、 蒸发食盐水 |
下列有关实验说法不正确的是( )
| A、在用简易量热计测定反应热时,可使用碎泡沫起隔热保温作用、环形玻璃搅拌棒进行搅拌使其充分反应、读取反应中温度计的最高温度、取2-3 次的实验平均值,以达到良好的实验效果 |
| B、纸上层析属于色谱分析法,其原理仅和“毛细现象”相关 |
| C、向1mL0.5mol?L-1AlCl3溶液中滴加2mL饱和NaF溶液,再滴加1mL 3.0mol?L-1 NH3?H2O溶液,无沉淀生成,说明Al3+更易与F-结合成AlF63-- |
| D、为了使过饱和溶液中析出晶体,可用玻璃棒摩擦与溶液接触处的试管壁 |
某种兴奋剂是奥运会上最早使用并最早被禁用,其结构简式如下:下列有关叙述正确的是( )
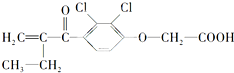

| A、该物质属于芳香族化合物,分子式为C13H12O4Cl2 |
| B、该物质分子内处于同一平面的碳原子不超过7个 |
| C、1 mol该物质最多可与5 mol H2发生加成反应 |
| D、1 mol该物质最多可与含3 mol NaOH的水溶液发生反应 |
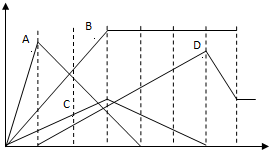 如图中,纵坐标为沉淀物的物质的量,横坐标为某溶液中加入反应物的物质的量,试按题意将相应图示的字母填入下表.
如图中,纵坐标为沉淀物的物质的量,横坐标为某溶液中加入反应物的物质的量,试按题意将相应图示的字母填入下表.