题目内容
10.符合图中阴影部分的物质是( )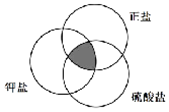
| A. | K2SO3 | B. | K2S2O3 | C. | K2 SO4 | D. | KHSO4 |
分析 酸跟碱完全中和生成的盐中,不会有酸中的氢离子,也不会有碱中的氢氧根离子,只有金属阳离子和酸根离子,这样的盐为正盐,含有钾离子的盐称为钾盐,含有硫酸根离子的盐成为硫酸盐,以此解答.
解答 解:A、K2SO3属于正盐、钾盐,但不属于硫酸盐,故A错误;
B、K2S2O3属于正盐、钾盐、硫代硫酸盐,故B错误;
C、K2SO4属于正盐、钾盐、硫酸盐,故C正确;
D、KHSO4属于酸式盐、钾盐、硫酸盐,故D错误;
故选C.
点评 本题考查物质的分类,分类的标准不一样,分类的结果就不一样,所以要严格按照定义去分类,掌握定义是关键.

练习册系列答案
 字词句篇与同步作文达标系列答案
字词句篇与同步作文达标系列答案
相关题目
20.下列说法正确的是( )
| A. | 放热反应在常温下一定是很容易发生 | |
| B. | 需要加热才能发生的反应一定是吸热反应 | |
| C. | 在稀溶液中,1 mol酸与1mol碱发生中和反应时所释放的热量叫中和热 | |
| D. | 一个反应是放热还是吸热,主要取决于反应物总能量与生成物总能量的相对大小 |
1.已知强酸与强碱的稀溶液发生中和反应的热化学方程式为H+(aq)+OH-(aq)═H2O(l)△H=-57.3kJ•mol-1,向0.1L 0.2mol•L-1的NaOH溶液中加入下列物质:①稀醋酸;②浓硫酸;③稀盐酸,恰好完全反应.则其焓变△H1、△H2、△H3的关系是( )
| A. | △H1>△H2>△H3 | B. | △H1>△H3>△H2 | C. | △H1=△H3>△H2 | D. | △H1<△H3<△H2 |
18.用NA表示阿伏加德罗常数的数值,下列叙述正确的是( )
| A. | 等质量的O2和O3中所含分子数相等 | |
| B. | 常温常压下,14g N2含有质子数为7NA | |
| C. | 标准状况下,22.4L H2含有的原子数为NA | |
| D. | 等质量的CO与CO2中所含碳原子数之比为7:11 |
5.下列说法不正确的是( )
| A. | 增加反应物浓度可以增加单位体积活化分子数目,但活化分子百分数保持不变 | |
| B. | 升高温度可以提高活化分子的百分数,从而提高反应速率 | |
| C. | 对于任何反应,压缩容器容积来增大压强,反应速率都加快 | |
| D. | 催化剂可以降低反应所需要的活化能,提高活化分子的百分数,从而提高反应速率 |
15.化学与人类生产、生活、社会可持续发展密切相关.下列有关说法正确的是( )
| A. | MgO和Al2O3在工业上用于制作耐高温材料,也可用于电解法冶炼Mg、Al | |
| B. | 水泥冶金厂常用高压电除去工厂烟尘,利用了胶体的性质 | |
| C. | 臭氧层吸收太阳紫外线,反应3O2=2O3有单质参加,属于氧化还原反应 | |
| D. | 向水中加入明矾进行杀菌消毒 |
2.用NA表示阿伏加德罗常数的值,下列叙述正确的是( )
| A. | 标准状况下,11.2LH2O含有的分子数为0.5NA | |
| B. | 在常温常压下,11.2LCl2含有的分子数为0.5NA | |
| C. | 25℃,1标准大气压下,64g SO2 中含有的原子数为3NA | |
| D. | 含有NA个氦原子的氦气在标准状况下的体积约为11.2L |