题目内容
18.用NA表示阿伏加德罗常数的数值,下列叙述正确的是( )| A. | 等质量的O2和O3中所含分子数相等 | |
| B. | 常温常压下,14g N2含有质子数为7NA | |
| C. | 标准状况下,22.4L H2含有的原子数为NA | |
| D. | 等质量的CO与CO2中所含碳原子数之比为7:11 |
分析 A、氧气和臭氧的摩尔质量不同;
B、求出氮气的物质的量,然后根据氮气中含14个质子来分析;
C、求出氢气的物质的量,然后根据氢气为双原子分子来分析;
D、CO与CO2的摩尔质量不同.
解答 解:A、氧气和臭氧的摩尔质量不同,故等质量的氧气和臭氧的物质的量不同,故分子个数不同,故A错误;
B、14g氮气的物质的量为0.5mol,而氮气中含14个质子,故0.5mol氮气中含7NA个原子,故B正确;
C、标况下22.4L氢气的物质的量为1mol,而氢气为双原子分子,故1mol氢气中含2mol原子即2NA个,故C错误;
D、CO与CO2的摩尔质量之比为28:44,故等质量的CO和二氧化碳的物质的量之比为44:28=11:7,故含有的碳原子之比为11:7,故D错误.
故选B.
点评 本题考查了阿伏伽德罗常数的有关计算,熟练掌握公式的使用和物质的结构是解题关键,难度不大.

练习册系列答案
相关题目
8.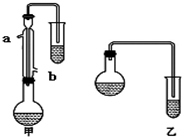 某化学小组以苯甲酸为原料,制取苯甲酸甲酯,已知有关物质的沸点如下表:
某化学小组以苯甲酸为原料,制取苯甲酸甲酯,已知有关物质的沸点如下表:
(1)甲和乙两位同学分别设计了如下图所示的两套实验室合成苯甲酸甲酯的装置(夹持仪器和加热仪器均已略去).根据有机物的沸点,最好采用甲(填“甲”或“乙”)装置.理由是甲中有冷凝回流装置.
(2)实验中浓硫酸的作用是催化剂、吸水剂.
(3)反应物CH3OH应过量,理由是反应物CH3OH过量,使平衡向右移动,有利于提高苯甲酸的转化率.
(4)苯甲酸甲酯粗产品中往往含有少量甲醇、苯甲酸和水等,现拟用下列流程图进行精制,请在流程图中方括号内填入操作方法的名称.
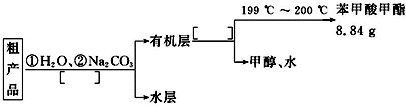
 某化学小组以苯甲酸为原料,制取苯甲酸甲酯,已知有关物质的沸点如下表:
某化学小组以苯甲酸为原料,制取苯甲酸甲酯,已知有关物质的沸点如下表:| 物质 | 甲醇 | 苯甲酸 | 苯甲酸甲酯 |
| 沸点/℃ | 64.7 | 249 | 199.6 |
(2)实验中浓硫酸的作用是催化剂、吸水剂.
(3)反应物CH3OH应过量,理由是反应物CH3OH过量,使平衡向右移动,有利于提高苯甲酸的转化率.
(4)苯甲酸甲酯粗产品中往往含有少量甲醇、苯甲酸和水等,现拟用下列流程图进行精制,请在流程图中方括号内填入操作方法的名称.

9.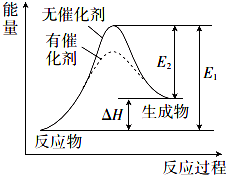 某反应的反应过程中能量变化如图所示(图中E1表示正反应的活化能,E2表示逆反应的活化能).下列说法错误的是( )
某反应的反应过程中能量变化如图所示(图中E1表示正反应的活化能,E2表示逆反应的活化能).下列说法错误的是( )
 某反应的反应过程中能量变化如图所示(图中E1表示正反应的活化能,E2表示逆反应的活化能).下列说法错误的是( )
某反应的反应过程中能量变化如图所示(图中E1表示正反应的活化能,E2表示逆反应的活化能).下列说法错误的是( )| A. | 该反应为吸热反应 | |
| B. | 催化剂不能改变反应的焓变(△H) | |
| C. | 催化剂能降低反应的活化能 | |
| D. | 逆反应的活化能大于正反应的活化能 |
6.现有三组溶液:①水和植物油的混合物 ②提取白酒中的乙醇 ③氯化钠和单质溴的混合液.分离以上各混合液的正确方法依次( )
| A. | 分液、萃取、蒸馏 | B. | 萃取、蒸馏、分液 | C. | 分液、蒸馏、萃取 | D. | 蒸馏、萃取、分液 |
13.下列有关化学用语表示正确的是( )
| A. | 对烃基苯甲醛的结构简式: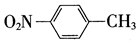 | B. | 质量数为37的氯原子:$\stackrel{37}{17}$Cl | ||
| C. | NH4Br的电子式: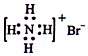 | D. | 二氧化碳分子的比例模型: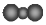 |
10.符合图中阴影部分的物质是( )
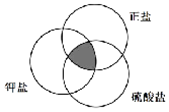

| A. | K2SO3 | B. | K2S2O3 | C. | K2 SO4 | D. | KHSO4 |
7.下列溶液中Cl-的物质的量最多的是( )
| A. | 200mL 2mol/L MgCl2溶液 | B. | 150mL 5mol/L KClO3溶液 | ||
| C. | 标准状况下,13.44L的HCl气体 | D. | 29.25gNaCl固体 |
8.实验室欲配制480mL浓度为0.1mol•L-1的Na2CO3溶液,下列操作可以实现的是( )
| A. | 称量5.3 g Na2CO3固体溶于480 mL水配制成溶液 | |
| B. | 称量5.3 g Na2CO3固体溶于水配制成0.5 L溶液 | |
| C. | 称量5.3 g Na2CO3•10H2O晶体溶于水配制成0.5 L溶液 | |
| D. | 称量5.3 g Na2CO3•10H2O晶体溶于0.5 L水配制成溶液 |