��Ŀ����
�й�ҽѧ������ܶѧ���ʺ���������ҹ�������ҽ���У��硶���ݸ�Ŀ���о��м��أ����̷���FeSO4?7H2O��������������Ҫҩ�ù����dz�ʪ���ⶾ��������ֹѪ����������ij��ѧ��ȤС���ͬѧ�������Ϻ���������м�����������������������ʣ�Ϊԭ�ϣ�����Ʊ������̷������̣�

����������Ϣ��С��ͬѧ��������̣��ش��������⣺
��1�������Ƶõ��̷��������Ƿ���Fe3+�����ѡ���Լ� ��
A��KSCN B��NaOH��Һ C��KmnO4 D����ˮ
��2����ҺA����Ҫ�ɷ��� ��
��3��������ͨ�����������͵���ҪĿ���� ������Һ����ϡ�������pH=2��Ŀ���� ��
��4������I������ʵ���������Ϊ����Ũ���� �� ��
��5�����������С��ͬѧΪ�ⶨ�̷���Ʒ��Fe2+��������ȡ2.850g�̷���Ʒ���ܽ����ó�250mL��Һ��ȡ25.00mL����Һ����ƿ�У�������ữ��0.010molL-1��KMnO4��Һ�ζ����յ㣬�ζ�����������KMnO4��Һ�����ƽ��ֵΪ20.00mL��
�ٵζ�ʱʢ��KMnO4��Һ������Ϊ �����������ƣ�
��������Ʒ��FeSO4?7H2O����������Ϊ ��

����������Ϣ��С��ͬѧ��������̣��ش��������⣺
��1�������Ƶõ��̷��������Ƿ���Fe3+�����ѡ���Լ�
A��KSCN B��NaOH��Һ C��KmnO4 D����ˮ
��2����ҺA����Ҫ�ɷ���
��3��������ͨ�����������͵���ҪĿ����
��4������I������ʵ���������Ϊ����Ũ����
��5�����������С��ͬѧΪ�ⶨ�̷���Ʒ��Fe2+��������ȡ2.850g�̷���Ʒ���ܽ����ó�250mL��Һ��ȡ25.00mL����Һ����ƿ�У�������ữ��0.010molL-1��KMnO4��Һ�ζ����յ㣬�ζ�����������KMnO4��Һ�����ƽ��ֵΪ20.00mL��
�ٵζ�ʱʢ��KMnO4��Һ������Ϊ
��������Ʒ��FeSO4?7H2O����������Ϊ
���㣺���ʷ�����ᴿ�ķ����ͻ��������ۺ�Ӧ��,�Ʊ�ʵ�鷽�������
ר�⣺ʵ�������
��������������м�����������������������ʣ�Ϊԭ�ϣ��Ʊ������̷�����Ϊ����������ϡ���ᣬ�������ᷴӦFe+H2SO4=FeSO4+H2�� ���������������������ᷴӦSn+H2SO4=SnSO4+H2���������������ᷴӦFe2O3+3H2SO4=Fe2��SO4��3+3H2O����������Ϊ����������Fe2��SO4��3+Fe=3FeSO4����������ҺAΪFeSO4��SnSO4��ͨ�����⣬����������������Һ����ϡ�������pH=2��������������ϡ���ᣬ�ɳ�ȥ��Һ�е�Sn2+���ӣ�ͬʱ�ɷ�ֹFe2+�������ɳ��������˳���Ϊ����������ҺBΪFeSO4��ͨ������Ũ���������ᾧ������ϴ�Ӹ���õ���Ʒ��
��1���������������ӵļ��鷽�������ش����������������������Һ��Ѫ��ɫ��
��2���������Ϸ�����ҺA����Ҫ�ɷ���FeSO4��SnSO4��
��3������������������ϡ���ᣬ������ˮ��pH=2Fe2+����δ���ɳ����������
��4����Ϊ�̷������ǽᾧˮ�������Ҫ����ҺD�еõ��̷����壬����ֱ�����ɣ�������е�ʵ����������ǣ�����Ũ������ȴ�ᾧ�����ˡ���Ȼ���
��5���ٸ�����ؾ���ǿ�����ԣ�������ζ��ܵĹ����𣻢ڸ���������ԭ��Ӧ�ļ���ԭ���ǵ��ӵ�ʧ������ȣ��ó�KMnO4��Fe2+�Ķ�Ӧ��ϵ����KMnO4���Fe2+��������Ϊ��Ʒ�����250mL��Һ���ζ�ʱȡ����25.00mL�����Գ���10��
��1���������������ӵļ��鷽�������ش����������������������Һ��Ѫ��ɫ��
��2���������Ϸ�����ҺA����Ҫ�ɷ���FeSO4��SnSO4��
��3������������������ϡ���ᣬ������ˮ��pH=2Fe2+����δ���ɳ����������
��4����Ϊ�̷������ǽᾧˮ�������Ҫ����ҺD�еõ��̷����壬����ֱ�����ɣ�������е�ʵ����������ǣ�����Ũ������ȴ�ᾧ�����ˡ���Ȼ���
��5���ٸ�����ؾ���ǿ�����ԣ�������ζ��ܵĹ����𣻢ڸ���������ԭ��Ӧ�ļ���ԭ���ǵ��ӵ�ʧ������ȣ��ó�KMnO4��Fe2+�Ķ�Ӧ��ϵ����KMnO4���Fe2+��������Ϊ��Ʒ�����250mL��Һ���ζ�ʱȡ����25.00mL�����Գ���10��
���
�⣺��1�����������̷��������Ƿ���Fe3+��ʵ��������������������Ӽ��鷽������������������������������ӻᷴӦ������������Ѫ��ɫ��֤�������ӵĴ��ڣ�
A��KSCN��Һ�����������ӷ�Ӧ����Ѫ��ɫ��Һ�����Լ��������ӵļ��飬��A���ϣ�
B��NaOH��Һ���������ӷ�Ӧ���ɰ�ɫ����Ѹ�ٱ仯Ϊ����ɫ����Ϊ���ɫ���������ӷ�Ӧ���ɺ��ɫ���������ܼ��������ӵĴ��ڣ���B�����ϣ�
C��KMnO4��Һ���������ӷ�Ӧ������������C�����ϣ�
D����ˮ�������ڼ���Fe3+��������Һ�к���Fe2+���ױ���������Ϊ�����Ӳ�����죬��D�����ϣ�
�ʴ�Ϊ��A��
��2��������м�����������������������ʣ�����������ϡ���ᣬ�������ᷴӦFe+H2SO4=FeSO4+H2�� ���������������������ᷴӦSn+H2SO4=SnSO4+H2���������������ᷴӦFe2O3+3H2SO4=Fe2��SO4��3+3H2O����������Ϊ����������Fe2��SO4��3+Fe=3FeSO4����������ҺAΪFeSO4��SnSO4��
�ʴ�Ϊ��FeSO4��SnSO4��
��3��ͨ�����⣬����������������Һ����ϡ�������pH=2��������������ϡ���ᣬ�ɳ�ȥ��Һ�е�Sn2+���ӣ�ͬʱ�ɷ�ֹFe2+�������ɳ��������˳���Ϊ��������
�ʴ�Ϊ����ȥ��Һ�е�Sn2+���ӣ���ֹFe2+�������ɳ�����
��4����Ϊ�̷������ǽᾧˮ�������Ҫ����ҺD�еõ��̷����壬����ֱ�����ɣ�������е�ʵ����������ǣ�����Ũ������ȴ�ᾧ�����ˡ���Ȼ���
�ʴ�Ϊ����ȴ�ᾧ������ϴ�Ӹ��
��5���ٸ�����ؾ���ǿ�����ԣ��������ܣ�ֻ��ʢ������ʽ�ζ����У�
�ʴ�Ϊ����ʽ�ζ��ܣ�
�ڸ��������������Һ�о���ǿ��������������������Ϊ�����ӣ���������ԭΪ�����ӣ����ݵ����غ��֪���������ӷ�ӦΪ��5Fe2++MnO4-+8H+=5Fe3++Mn2++4H2O��KMnO4��5Fe2+��FeSO4?7H2O����Ħ������Ϊ278g/mol��2.850g�̷���Ʒ����Ʒ�к�FeSO4?7H2O��0.02L��0.01mol/L��5��10��278g/mol=2.78g�������Ʒ��FeSO4?7H2O����������Ϊ
��100%=97.5%��
�ʴ�Ϊ��97.5%��
A��KSCN��Һ�����������ӷ�Ӧ����Ѫ��ɫ��Һ�����Լ��������ӵļ��飬��A���ϣ�
B��NaOH��Һ���������ӷ�Ӧ���ɰ�ɫ����Ѹ�ٱ仯Ϊ����ɫ����Ϊ���ɫ���������ӷ�Ӧ���ɺ��ɫ���������ܼ��������ӵĴ��ڣ���B�����ϣ�
C��KMnO4��Һ���������ӷ�Ӧ������������C�����ϣ�
D����ˮ�������ڼ���Fe3+��������Һ�к���Fe2+���ױ���������Ϊ�����Ӳ�����죬��D�����ϣ�
�ʴ�Ϊ��A��
��2��������м�����������������������ʣ�����������ϡ���ᣬ�������ᷴӦFe+H2SO4=FeSO4+H2�� ���������������������ᷴӦSn+H2SO4=SnSO4+H2���������������ᷴӦFe2O3+3H2SO4=Fe2��SO4��3+3H2O����������Ϊ����������Fe2��SO4��3+Fe=3FeSO4����������ҺAΪFeSO4��SnSO4��
�ʴ�Ϊ��FeSO4��SnSO4��
��3��ͨ�����⣬����������������Һ����ϡ�������pH=2��������������ϡ���ᣬ�ɳ�ȥ��Һ�е�Sn2+���ӣ�ͬʱ�ɷ�ֹFe2+�������ɳ��������˳���Ϊ��������
�ʴ�Ϊ����ȥ��Һ�е�Sn2+���ӣ���ֹFe2+�������ɳ�����
��4����Ϊ�̷������ǽᾧˮ�������Ҫ����ҺD�еõ��̷����壬����ֱ�����ɣ�������е�ʵ����������ǣ�����Ũ������ȴ�ᾧ�����ˡ���Ȼ���
�ʴ�Ϊ����ȴ�ᾧ������ϴ�Ӹ��
��5���ٸ�����ؾ���ǿ�����ԣ��������ܣ�ֻ��ʢ������ʽ�ζ����У�
�ʴ�Ϊ����ʽ�ζ��ܣ�
�ڸ��������������Һ�о���ǿ��������������������Ϊ�����ӣ���������ԭΪ�����ӣ����ݵ����غ��֪���������ӷ�ӦΪ��5Fe2++MnO4-+8H+=5Fe3++Mn2++4H2O��KMnO4��5Fe2+��FeSO4?7H2O����Ħ������Ϊ278g/mol��2.850g�̷���Ʒ����Ʒ�к�FeSO4?7H2O��0.02L��0.01mol/L��5��10��278g/mol=2.78g�������Ʒ��FeSO4?7H2O����������Ϊ
| 2.78 |
| 2.85 |
�ʴ�Ϊ��97.5%��
�����������ۺϿ������ʵ��Ʊ�������̽����֪ʶ��������ѧ���ķ���������ʵ�������Ŀ��飬Ϊ�߿��������ͣ�ע�����ʵ��IJ���ԭ���Ͳ��裬����������ʵ����ʣ���Ŀ�Ѷ��еȣ�

��ϰ��ϵ�д�
 ��У����ϵ�д�
��У����ϵ�д�
�����Ŀ
��������ʵ�Ľ��ͣ���Ӧ�����ӷ���ʽ��ȷ���ǣ�������
| A����������һ�ֶ�Ԫ���H2S?S2-+2H+ |
| B����ҵ��FeCl3��Һ��ʴͭ�����壺2Fe3-+Cu?2Fe2++Cu2+ |
| C��Al����NaOH��Һ��2Al+2OH-=2AlO2-+H2�� |
| D����ʳ�׳�ȥˮ���е�ˮ��2H++CaCO3=Ca2-+H2O+CO2 |
1.92gͭ����һ����Ũ���ᷴӦ��ͭ����ȫ�ܽ⣬�õ�����1.12L�������������������������ʵ�����������
| A��0.12mol |
| B��0.11mol |
| C��0.99mol |
| D��0.08mol |
���к�������������ǿ���ǣ�������
| A��H3PO4 |
| B��H3AsO4 |
| C��HNO3 |
| D��HClO |
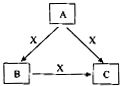
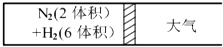 ��һ�����¶��£���2���N2��6���H2�ֱ�ͨ��һ��������������ɱ�������У�������һ���������ͨ�����з������·�Ӧ��N2��g��+3H2��g��?2NH3��g����H��0 ��Ӧ�ﵽƽ���û������Ϊ7�����
��һ�����¶��£���2���N2��6���H2�ֱ�ͨ��һ��������������ɱ�������У�������һ���������ͨ�����з������·�Ӧ��N2��g��+3H2��g��?2NH3��g����H��0 ��Ӧ�ﵽƽ���û������Ϊ7�����