题目内容
6.已知2H2(g)+O2(g)→2H2O(g)+483.6kJ.下列说法正确的是( )| A. | 1mol氢气完全燃烧生成液态水放出的热量小于241.8KJ | |
| B. | 1mol水蒸气完全分解成氢气与氧气,需吸收241.8kJ热量 | |
| C. | 2mol氢气与1mol氧气的总能量小于2mol 水蒸气的总能量 | |
| D. | 2mol氢氢键和1mol氧氧键拆开所消耗的能量大于4mol氢氧键成键所放出的能量 |
分析 A、水蒸气转化为液态水的过程是放热过程,据此回答;
B、互为逆过程的两个反应的焓变互为相反数;
C、反应是放热的,所以反应物的能量高于产物的能量;
D、化学反应的焓变等于旧件断裂吸收的能量和新键生成释放的能量的差值.
解答 解:由氢气燃烧的热化学方程式可知,2mol氢气与1mol氧气燃烧生成2mol水蒸气放热483.6KJ,
A、水蒸气转化为液态水的过程是放热过程,1mol氢气完全燃烧生成液态水放出的热量大于241.8KJ,故A错误;
B、氢气的燃烧热是1mol氢气燃烧指生成1mol液态水时放出的热量,故B正确;
C、水由气态转变为液态也要放热,所以2mol H2完全燃烧生成液态水放出的热量大于483.6 kJ,故C错误;
D、该反应为放热反应,则形成2 mol H2O的化学键释放的总能量大于断裂2 mol H2和1 mol O2 的化学键所吸收的总能量,故D错误;
故选B.
点评 本题考查燃烧热的热化学反应方程式,明确燃烧的概念及反应热与键能的关系即可解答,题目难度不大.

练习册系列答案
 各地期末复习特训卷系列答案
各地期末复习特训卷系列答案 小博士期末闯关100分系列答案
小博士期末闯关100分系列答案
相关题目
16.现有1950g发烟硫酸(用a SO3•H2O 表示),SO3和H2SO4的质量分数分别为0.2和0.8,加b g水稀释成某浓度的硫酸(用H2SO4•$\frac{1}{9}$H2O 表示),则以下正确的是(允许最后一位数字不同)( )
| A. | a=1.38 | B. | a=1.31 | C. | b=174 | D. | b=129 |
17.类比推断是学习化学的一种重要方法,推断正确的是( )
| A. | 电解熔融NaCl制取Na,故电解熔融MgCl2也能制取Mg | |
| B. | Fe与CuSO4溶液反应置换出Cu,故Na也能从CuSO4溶液中置换出Cu | |
| C. | 通常元素的价态越高对应物质的氧化性越强,故HClO4的氧化性强于HClO | |
| D. | CO2和Na2O2反应生成Na2CO3和O2,故SO2和Na2O2反应生成Na2SO3和O2 |
1.常温下非固态的物质是( )
| A. | 软脂酸(C15H31COOH) | B. | 油酸(C17H33COOH) | ||
| C. | 草酸(HOOC-COOH) | D. | 氨基酸(H2N-CH2COOH) |
11.观察如图装置,下列说法正确的是( )
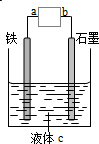

| A. | a、b接电流表,该装置为原电池 | |
| B. | a、b接直流电源,该装置为电解池 | |
| C. | a、b接直流电源,铁可能不易被腐蚀 | |
| D. | a、b接电流表或接直流电源,铁都可能是负极 |
15.下列说法正确的是( )
| A. | 某温度时,KW=10-12,此温度下PH=6的溶液一定显酸性 | |
| B. | 25℃时,0.1mol/L的NaHSO3溶液pH=4,说明HSO3-在水溶液中只存在电离 | |
| C. | NH4Cl、CH3COONa、NaHCO3、NaHSO4溶于水,对水的电离都有促进作用 | |
| D. | 稀释 0.1mol/L CH3COONa溶液过程中,c(OH-)/c(CH3COO-)增大 |
16.现有某氯化物与氯化镁的混合物,取3.8g粉末完全溶于水后,与足量的硝酸银溶液反应后得到12.4g氯化银沉淀,则该混合物中的另一氯化物是( )
| A. | AlCl3 | B. | KCl | C. | CaCl2 | D. | LiCl |
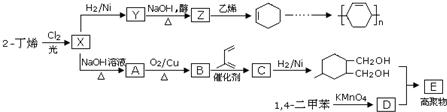
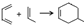 .
.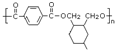 ;甲是A的一种同分异构体,其能实现转化:
;甲是A的一种同分异构体,其能实现转化: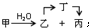 ,甲的名称为乙酸乙酯;
,甲的名称为乙酸乙酯;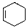 可以合成
可以合成 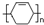 .按合成路线的顺序,涉及反应的反应类型有:加成、消去、加聚.
.按合成路线的顺序,涉及反应的反应类型有:加成、消去、加聚. 氯化铝可制备无机高分子混凝剂,在有机合成中有广泛的用途.
氯化铝可制备无机高分子混凝剂,在有机合成中有广泛的用途.