题目内容
已知CuSO4溶液分别与Na2CO3溶液、Na2S溶液的反应情况如下:
(1)CuSO4+Na2CO3主要:Cu2++CO32-+H2O→Cu(OH)2↓+CO2↑次要:Cu2++CO32-→CuCO3↓
(2)CuSO4+Na2S主要:Cu2++S2-→CuS↓次要:Cu2++S2-+2H2O→Cu(OH)2↓+H2S↑
下列几种物质的溶解度大小的比较中,正确的是( )
(1)CuSO4+Na2CO3主要:Cu2++CO32-+H2O→Cu(OH)2↓+CO2↑次要:Cu2++CO32-→CuCO3↓
(2)CuSO4+Na2S主要:Cu2++S2-→CuS↓次要:Cu2++S2-+2H2O→Cu(OH)2↓+H2S↑
下列几种物质的溶解度大小的比较中,正确的是( )
| A、Cu(OH)2>CuCO3>CuS |
| B、CuS>Cu(OH)2>CuCO3 |
| C、CuS<Cu(OH)2<CuCO3 |
| D、Cu(OH)2<CuCO3<CuS |
考点:难溶电解质的溶解平衡及沉淀转化的本质
专题:电离平衡与溶液的pH专题
分析:沉淀反应中,生成物的溶解度越小,沉淀反应越容易发生.根据信息(1)可知:生成Cu(OH)2的反应容易发生,说明Cu(OH)2的溶解度小于CuCO3的溶解度;
根据信息(2)可知:生成CuS的反应容易发生,说明CuS的溶解度小于Cu(OH)2的溶解度,以此解答该题.
根据信息(2)可知:生成CuS的反应容易发生,说明CuS的溶解度小于Cu(OH)2的溶解度,以此解答该题.
解答:
解:沉淀反应中,生成物的溶解度越小,沉淀反应越容易发生,
CuSO4+Na2CO3中主要发生Cu2++CO32─+H2O=Cu(OH)2↓+CO2↑,次要发生Cu2++CO32─=CuCO3↓,可说明Cu(OH)2的溶解度小于CuCO3的溶解度;
CuSO4+Na2S中主要:Cu2++S2─=CuS↓,次要:Cu2++S2─+2H2O=Cu(OH)2↓+H2S↑,可说明CuS的溶解度小于Cu(OH)2的溶解度,
则溶解度CuS<Cu(OH)2<CuCO3,
故选C.
CuSO4+Na2CO3中主要发生Cu2++CO32─+H2O=Cu(OH)2↓+CO2↑,次要发生Cu2++CO32─=CuCO3↓,可说明Cu(OH)2的溶解度小于CuCO3的溶解度;
CuSO4+Na2S中主要:Cu2++S2─=CuS↓,次要:Cu2++S2─+2H2O=Cu(OH)2↓+H2S↑,可说明CuS的溶解度小于Cu(OH)2的溶解度,
则溶解度CuS<Cu(OH)2<CuCO3,
故选C.
点评:本题考查难溶电解质的溶解平衡,题目难度不大,注意理解溶解度小的沉淀易转化为溶解度更小的沉淀的规律,为解答该题的关键.

练习册系列答案
相关题目
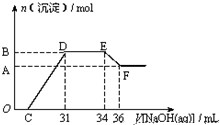 某同学取一定量Fe与Al的混合物与一定量极稀的硝酸充分反应,已知硝酸的还原产物仅有一种,在反应结束后的溶液中,逐滴加入4mol?L-1的氢氧化钠溶液,所加氢氧化钠溶液的体积(mL)与产生的沉淀的物质的量(mol)的关系如图所示,试分析硝酸被还原后生成的产物为( )
某同学取一定量Fe与Al的混合物与一定量极稀的硝酸充分反应,已知硝酸的还原产物仅有一种,在反应结束后的溶液中,逐滴加入4mol?L-1的氢氧化钠溶液,所加氢氧化钠溶液的体积(mL)与产生的沉淀的物质的量(mol)的关系如图所示,试分析硝酸被还原后生成的产物为( )| A、NH4NO3 |
| B、NO2 |
| C、NO |
| D、N2O3 |
下列有关叙述正确的是( )
A、氨水与氯化铵的pH=7的混合溶液中:c(Cl-)>c(NH
| ||
| B、pH=2的一元酸和pH=12的一元强碱等体积混合:c(OH-)=c(H+) | ||
C、室温下向10 mL pH=3的醋酸溶液中加水稀释,溶液中
| ||
| D、在0.1 mol?L-1的硫化钠溶液中,c(OH-)=c(H+)+c(HS-)+c(H2S) |
下列实验I~Ⅳ中,正确的是( )


| A、实验Ⅰ:配置一定物质的量浓度的溶液 |
| B、实验Ⅱ:除去Cl2中的HCl |
| C、实验Ⅲ:用水吸收NH3 |
| D、实验Ⅳ:石油的分馏 |
对下列各组物质关系的描述中正确的是( )
A、 与 与 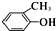 属于同素异形体 属于同素异形体 |
| B、CH3COOH与硬脂酸(C17H35COOH)属于同系物 |
C、 与 与  属于同一种物质 属于同一种物质 |
D、 与 与 属于同分异构体 属于同分异构体 |