题目内容
18.下列排列顺序中,不正确的是( )| A. | 酸性:HClO<H2SO3<HClO4 | B. | 稳定性:PH3<H2S<NH3 | ||
| C. | 电负性:P<S<Cl | D. | 沸点:HF<HBr<HI |
分析 A.HClO4为强酸,亚硫酸为中强酸,HClO为弱酸;
B.非金属性越强,对应氢化物越稳定;
C.非金属性越强,电负性越大;
D.HF分子间含氢键,沸点最高,相对分子质量越大的分子的沸点高.
解答 解:A.HClO4为强酸,亚硫酸为中强酸,HClO为弱酸,则酸性:HClO<H2SO3<HClO4,故A正确;
B.非金属性P<S<N,则稳定性:PH3<H2S<NH3,故B正确;
C.非金属性P<S<Cl,则电负性P<S<Cl,故C正确;
D.HF分子间含氢键,沸点最高,相对分子质量越大的分子的沸点高,则沸点为HBr<HI<HF,故D错误;
故选D.
点评 本题考查元素周期表和周期律,为高频考点,把握元素的位置、性质、元素周期律为解答的关键,侧重分析与应用能力的考查,注意规律性知识的应用,题目难度不大.

练习册系列答案
相关题目
8.CO2和氢氧化钠溶液反应,所得产物中Na2CO3和NaHCO3物质的量之比为3:5,则参加反应的CO2和NaOH的物质的量之比为( )
| A. | 3:5 | B. | 1:2 | C. | 8:11 | D. | 18:8 |
6.下列说法正确的是( )
| A. | 1 mol H2SO4与 1 mol Ba(OH)2完全反应放出的热量叫做中和热 | |
| B. | 用弱酸的稀溶液做中和热测定实验,测得中和反应反应热偏大 | |
| C. | 一定量H2燃烧生成气态水时比生成液态水时放出的热量多 | |
| D. | 在101 kPa时,1 molH2在Cl2中燃烧时放出的热量也是H2的燃烧热 |
13.0.1mol/L CH3COONa溶液中,下列关系正确的是( )
| A. | c(H+)=c(OH-) | B. | c(CH3COOH)+c(CH3COO-)=0.1 mol/L | ||
| C. | c(CH3COOH)>c(CH3COO-) | D. | c(H+)>c(OH-) |
10.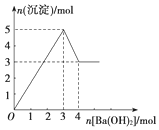 如图表示向某溶液中滴加Ba(OH)2溶液时,沉淀的物质的量随Ba(OH)2的物质的量的变化关系.该溶液的成分可能是( )
如图表示向某溶液中滴加Ba(OH)2溶液时,沉淀的物质的量随Ba(OH)2的物质的量的变化关系.该溶液的成分可能是( )
 如图表示向某溶液中滴加Ba(OH)2溶液时,沉淀的物质的量随Ba(OH)2的物质的量的变化关系.该溶液的成分可能是( )
如图表示向某溶液中滴加Ba(OH)2溶液时,沉淀的物质的量随Ba(OH)2的物质的量的变化关系.该溶液的成分可能是( )| A. | MgSO4 | B. | Al2(SO4)3 | C. | FeSO4 | D. | NaAlO2 |
7.下列各组离子在指定溶液中一定能大量共存的是( )
| A. | 能使酚酞试液变红的溶液中:H+、SO42-、Na+、NO3- | |
| B. | 加入Al能放出氢气的溶液中:NH4+、SO42-、Mg2+、HCO3- | |
| C. | 含有大量Cl2的溶液中:Ba2+、K+、NO3-、I- | |
| D. | 强酸性的溶液中:Cu2+、Br-、Ca2+、Cl- |
8.下列各组中的物质均能发生加成反应的是( )
| A. | 乙烯和乙醇 | B. | 苯和氯乙烯 | C. | 乙酸和溴乙烷 | D. | 丙烯和聚丙烯 |