题目内容
7.下列各组离子在指定溶液中一定能大量共存的是( )| A. | 能使酚酞试液变红的溶液中:H+、SO42-、Na+、NO3- | |
| B. | 加入Al能放出氢气的溶液中:NH4+、SO42-、Mg2+、HCO3- | |
| C. | 含有大量Cl2的溶液中:Ba2+、K+、NO3-、I- | |
| D. | 强酸性的溶液中:Cu2+、Br-、Ca2+、Cl- |
分析 A.能使酚酞试液变红的溶液中存在大量氢氧根离子,氢离子与氢氧根离子反应;
B.加入Al能放出氢气的溶液中存在大量氢离子或氢氧根离子,铵根离子、镁离子、碳酸氢根离子与氢氧根离子反应,碳酸氢根离子与氢离子反应;
C.氯气具有强氧化性,能够氧化碘离子;
D.强酸性溶液中存在大量氢离子,四种离子之间不反应,都不与氢离子反应.
解答 解:A.能使酚酞试液变红的溶液呈碱性,溶液中存在大量氢氧根离子,H+与氢氧根离子反应,在溶液中不能大量共存,故A错误;
B.加入Al能放出氢气的溶液呈酸性或强碱性,NH4+、Mg2+、HCO3-与氢氧根离子反应,HCO3-与氢离子反应,在溶液中不能大量共存,故B错误;
C.Cl2、I-之间发生氧化还原反应,在溶液中不能大量共存,故C错误;
D.强酸性的溶液中存在大量氢离子,Cu2+、Br-、Ca2+、Cl-之间不反应,都不与氢离子反应,在溶液中能够大量共存,故D正确;
故选D.
点评 本题考查离子共存的判断,为高考的高频题,题目难度不大,注意明确离子不能大量共存的一般情况:能发生复分解反应的离子之间;能发生氧化还原反应的离子之间等;还应该注意题目所隐含的条件,如:溶液的酸碱性,据此来判断溶液中是否有大量的 H+或OH-;溶液的颜色,如无色时可排除 Cu2+、Fe2+、Fe3+、MnO4-等有色离子的存在;溶液的具体反应条件,如“氧化还原反应”、“加入铝粉产生氢气”;是“可能”共存,还是“一定”共存等.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
17.由苯和乙醛组成的混合液体,经测定其中碳的质量分数为72%,则混合物中氧元素的质量分数为( )
| A. | 2.14% | B. | 19.56% | C. | 22.65% | D. | 32.00% |
18.下列排列顺序中,不正确的是( )
| A. | 酸性:HClO<H2SO3<HClO4 | B. | 稳定性:PH3<H2S<NH3 | ||
| C. | 电负性:P<S<Cl | D. | 沸点:HF<HBr<HI |
2.下列有关化学用语表示正确的是( )
| A. | H2O2的电子式: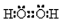 | |
| B. | 次氯酸分子的结构式:H-Cl-O | |
| C. | 乙醇的分子式:C2H5OH | |
| D. | 1,1-二溴乙烷的结构简式:CH3CHBr2 |
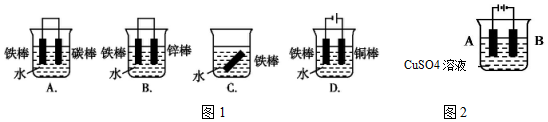
19.下列各装置能构成原电池的是( )
| A. |  | B. |  | C. |  | D. |  |
 AsH3分子的VSEPR模型名称四面体结构,立体构型名称为三角锥,含有的共价键为极性键(极性键,非极性键),属于极性分子(极性分子,非极性分子),砷原子采取sp3杂化.
AsH3分子的VSEPR模型名称四面体结构,立体构型名称为三角锥,含有的共价键为极性键(极性键,非极性键),属于极性分子(极性分子,非极性分子),砷原子采取sp3杂化.