题目内容
13.0.1mol/L CH3COONa溶液中,下列关系正确的是( )| A. | c(H+)=c(OH-) | B. | c(CH3COOH)+c(CH3COO-)=0.1 mol/L | ||
| C. | c(CH3COOH)>c(CH3COO-) | D. | c(H+)>c(OH-) |
分析 CH3COONa为强碱弱酸盐,水解显碱性,则c(H+)<c(OH-),结合水解程度不大及物料守恒式来解答.
解答 解:A.水解显碱性,则c(H+)<c(OH-),故A错误;
B.由物料守恒可知,c(CH3COOH)+c(CH3COO-)=c(Na+)=0.1 mol/L,故B正确;
C.由水解程度不大,可知c(CH3COOH)<c(CH3COO-),故C错误;
D.水解显碱性,则c(H+)<c(OH-),故D错误;
故选B.
点评 本题考查离子浓度的比较,为高频考点,把握水解应用及物料守恒为解答的关键,侧重分析与应用能力的考查,注意单一离子水解的程度不大,题目难度不大.

练习册系列答案
相关题目
3.向a mL0.25mol•L-1的AlCl3溶液中加入金属钠,反应完全后,恰好只形成NaCl和NaAlO2的混合溶液,则加入金属钠的物质的量为( )
| A. | 2.5a×10-4mol | B. | a×10-3mol | C. | 7.5a×10-4mol | D. | a×10-4mol |
4.用NA表示阿伏加德罗常数的值,下列说法正确的是( )
| A. | 2.4g镁变成Mg2+时失去的电子数目为0.2NA | |
| B. | 常温常压下,11.2L氧气所含的O原子数为NA | |
| C. | 如果11.2LN2中含有n个分子,则阿伏加德罗常数一定为2n | |
| D. | 1 mol•L-1的KSCN和1mol•L-1KAl(SO4)2溶液中,所含K+数都是NA |
1.下列关于金属钠的叙述中,说法正确的是( )
| A. | 钠在空气中燃烧,发出黄色火焰 | |
| B. | 钠在空气中燃烧,产物是Na2O | |
| C. | 钠是银白色金属,硬度大,熔点高 | |
| D. | 取用金属钠时,剩余的钠不能放回原瓶 |
18.下列排列顺序中,不正确的是( )
| A. | 酸性:HClO<H2SO3<HClO4 | B. | 稳定性:PH3<H2S<NH3 | ||
| C. | 电负性:P<S<Cl | D. | 沸点:HF<HBr<HI |
2.下列有关化学用语表示正确的是( )
| A. | H2O2的电子式: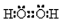 | |
| B. | 次氯酸分子的结构式:H-Cl-O | |
| C. | 乙醇的分子式:C2H5OH | |
| D. | 1,1-二溴乙烷的结构简式:CH3CHBr2 |
3.“绿色化学”是当今社会提出的一个新概念.在“绿色化学”工艺中,理想状态是反应中原子全部转化为目标产物,即原子利用率为100%.利用以下各种化学反应类型的合成过程最符合绿色化学的是( )
| A. | 取代反应 | B. | 水解反应 | C. | 加聚反应 | D. | 缩聚反应 |