题目内容
下列说法不正确的是( )
| A、将盐酸、KSCN溶液和Fe(NO3)2溶液三种溶液混合,混合溶液显红色 |
| B、SO2通入Fe2(SO4)3溶液中,无明显现象 |
| C、SO2通入已酸化的Ba(NO3)2溶液中,出现白色沉淀 |
| D、在滴有酚酞的Na2CO3溶液中,加入BaCl2溶液后红色褪去 |
考点:二价Fe离子和三价Fe离子的检验,二氧化硫的化学性质
专题:
分析:A.铁离子遇KSCN溶液,溶液为血红色;
B.SO2与Fe2(SO4)3溶液反应生成亚铁离子;
C.酸性条件下NO3-与SO2发生氧化还原反应生成SO42-;
D.Na2CO3为强碱弱酸盐,水解呈碱性.
B.SO2与Fe2(SO4)3溶液反应生成亚铁离子;
C.酸性条件下NO3-与SO2发生氧化还原反应生成SO42-;
D.Na2CO3为强碱弱酸盐,水解呈碱性.
解答:
解:A.盐酸和Fe(NO3)2溶液混合后发生氧化还原反应生成铁离子,铁离子遇KSCN溶液,溶液为血红色,故A正确;
B.SO2与Fe2(SO4)3溶液发生氧化还原反应生成亚铁离子,溶液变成浅绿色,故B错误;
C.酸性条件下NO3-与SO2发生氧化还原反应生成SO42-,生成的沉淀为BaSO4,故C正确;
D.Na2CO3为强碱弱酸盐,水解呈碱性,加入氯化钡生成碳酸钡沉淀,溶液后红色褪去,故D正确;
故选B.
B.SO2与Fe2(SO4)3溶液发生氧化还原反应生成亚铁离子,溶液变成浅绿色,故B错误;
C.酸性条件下NO3-与SO2发生氧化还原反应生成SO42-,生成的沉淀为BaSO4,故C正确;
D.Na2CO3为强碱弱酸盐,水解呈碱性,加入氯化钡生成碳酸钡沉淀,溶液后红色褪去,故D正确;
故选B.
点评:本题考查物质的性质,明确发生的化学反应是解答本题的关键,侧重于学生的分析能力、实验能力和评价能力的考查,难度中等.

练习册系列答案
 同步轻松练习系列答案
同步轻松练习系列答案 课课通课程标准思维方法与能力训练系列答案
课课通课程标准思维方法与能力训练系列答案
相关题目
下列现象不能用盐类水解知识解释的是( )
| A、明矾能用于净水 |
| B、泡沫灭火器的原理 |
| C、铜绿的生成 |
| D、配置FeCl2溶液时加入少量的盐酸 |
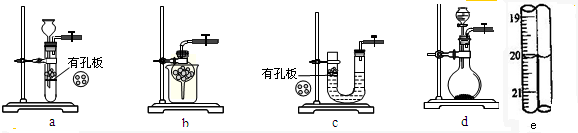
有一支50mL酸式滴定管,其中盛有溶液,液面恰好在10.00mL刻度处.把滴定管中的溶液全部排出,其体积( )
| A、大于40. 00 mL |
| B、等于40.00 mL |
| C、大于10.00 mL |
| D、等于10.00 mL |
反应N2(g)+O2(g)?2NO(g)在恒容密闭容器中进行,达到平衡后,充入N2,下列说法正确的是( )
| A、平衡向逆反应方向移动,N2和O2的转化率都减小 |
| B、平衡向正反应方向移动,N2和O2的转化率都增大 |
| C、压强增大平衡不移动,N2的转化率不变 |
| D、平衡向正反应方向移动,N2的转化率减小,O2的转化率增大 |
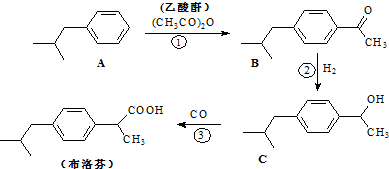

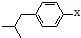 结构的酯类中共有6种(即X有不同的结构),请写出其中的二种
结构的酯类中共有6种(即X有不同的结构),请写出其中的二种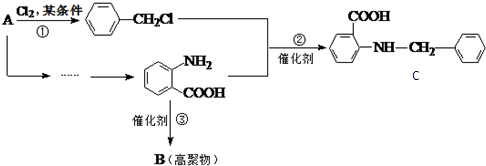

 中官能团的名称
中官能团的名称 多一个碳的同系物,则满足下列条件的D的同分异构体共有
多一个碳的同系物,则满足下列条件的D的同分异构体共有