题目内容
有一支50mL酸式滴定管,其中盛有溶液,液面恰好在10.00mL刻度处.把滴定管中的溶液全部排出,其体积( )
| A、大于40. 00 mL |
| B、等于40.00 mL |
| C、大于10.00 mL |
| D、等于10.00 mL |
考点:过滤、分离与注入溶液的仪器
专题:
分析:滴定管的“0”刻度在上、满刻度在下(量筒与此相反),在刻度以下还有一段空间没有刻度.
解答:
解:滴定管的“0”刻度在上、满刻度在下(量筒与此相反),在刻度以下还有一段空间没有刻度.因此,将装到50ml刻度处的溶液全部放出,除由10ml刻度处到50ml刻度处有40mL溶液外,还有满刻度以下的溶液一并放出,总量超过40mL.
故选A.
故选A.
点评:本题考查滴定管的结构,题目难度不大,注意滴定管的“0”刻度在上、满刻度在下(量筒与此相反),满刻度以下还有一段空间没有刻度.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
一定质量的铁、氧化铁、氧化铜的混合物粉末放入100mL4.40mol/L盐酸中,充分反应后产生896mL H2(标准状况),残留固体1.28g.过滤,滤液中无Cu2+,将滤液加水稀释到200mL,测得其中c(H+)为0.40mol/L.则原混合物中单质铁的质量是( )
| A、2.4g |
| B、10.08g |
| C、3.36g |
| D、5.60g |
下列说法不正确的是( )
| A、将盐酸、KSCN溶液和Fe(NO3)2溶液三种溶液混合,混合溶液显红色 |
| B、SO2通入Fe2(SO4)3溶液中,无明显现象 |
| C、SO2通入已酸化的Ba(NO3)2溶液中,出现白色沉淀 |
| D、在滴有酚酞的Na2CO3溶液中,加入BaCl2溶液后红色褪去 |
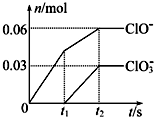 将一定量的Cl2通入一定浓度的苛性钾溶液中,两者恰好完全反应(已知反应过程放热),生成物中有三种含氯元素的离子,其中ClO-和ClO3-两种离子的物质的量(n)与反应时间(t)的变化示意图如图所示.下列说法不正确的是( )
将一定量的Cl2通入一定浓度的苛性钾溶液中,两者恰好完全反应(已知反应过程放热),生成物中有三种含氯元素的离子,其中ClO-和ClO3-两种离子的物质的量(n)与反应时间(t)的变化示意图如图所示.下列说法不正确的是( )| A、反应中转移电子的物质的量是0.21 mol |
| B、ClO3-的生成是由于温度升高引起的 |
| C、苛性钾溶液中KOH的质量为5.04g |
| D、反应中氧化剂和还原剂的物质的量之比为7:3 |
下列物质的溶液中通入过量CO2气体,其过程中不会有沉淀现象产生的是( )
| A、Na2SiO3 |
| B、NaAlO2 |
| C、饱和碳酸钠 |
| D、Ba(NO3)2 |
下列物质性质与应用对应关系正确的是( )
| A、过氧化钠可以与CO2反应放出O2,可用于潜艇中的供氧剂 |
| B、硅酸钠溶液呈碱性,可涂在木材的表面作耐火剂 |
| C、SO2具有氧化性,可用于纸浆的漂白 |
| D、明矾溶于水可形成有氢氧化铝胶体,可用于自来水的杀菌消毒 |
下列物质互为同分异构体的一组是( )
| A、氧气与臭氧 |
| B、1H和2H |
| C、甲烷和乙烷 |
| D、乙醇(CH3CH2OH)和甲醚(CH3OCH3) |
用酒精灯加热下列溶液,蒸干后灼烧,所得固体与原溶质相同的是( )
| A、FeCl3溶液 |
| B、NaHCO3溶液 |
| C、Na2SO3溶液 |
| D、Na2SO4溶液 |