题目内容
1.有A、B两种烃,其相关信息如下| A | 完全燃烧的产物中n(CO2):n(H2O)=2:1 28<Mr(A)<60 不能使溴的四氯化碳溶液褪色 一氯代物只有1种结构 |
| B | 饱和链烃,通常情况下呈气态 二溴代物有3种 |
(1)烃A的最简式是CH;
(2)烃A的结构简式是
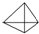 ;
;(3)烃B的3种二溴代物的结构简式为CHBr2CH(CH3)2;CH2BrCBr(CH3)2;CH2BrCH(CH3)CH2Br.
分析 A完全燃烧的产物中n(CO2):n(H2O)=2:1,故A的组成可以表示为(CH)n,由于28<M(A)<60,故28<13n<60,解得2.2<n<4.7,不能使溴的四氯化碳溶液褪色,说明分子中不含不饱和键,一氯代物只有一种结构,说明分子中H原子为等效H原子,不能使溴的四氯化碳溶液褪色,故碳碳之间都是单键,故n=4,为正四面体结构,A为 ;
;
B是饱和链烃,通常情况下呈气态,碳原子数目小于5(新戊烷除外),有同分异构体,碳原子数目大于3,二溴代物有三种为,故B为CH(CH3)3,据此解答.
解答 解:A完全燃烧的产物中n(CO2):n(H2O)=2:1,故A的组成可以表示为(CH)n,由于28<M(A)<60,故28<13n<60,解得2.2<n<4.7,不能使溴的四氯化碳溶液褪色,说明分子中不含不饱和键,一氯代物只有一种结构,说明分子中H原子为等效H原子,碳碳之间都是单键,故n=4,A分子式为C4H4,为正四面体结构,A为 ;
;
B是饱和链烃,通常情况下呈气态,碳原子数目小于5(新戊烷除外),有同分异构体,碳原子数目大于3,二溴代物有三种为,故B为CH(CH3)3,
(1)A分子式为C4H4,最简式是CH,故答案为:CH;
(2)由上述分析可知,烃A的结构简式是 ,故答案为:
,故答案为: ;
;
(3)B为CH(CH3)3,三种二溴代物的结构简式为:CHBr2CH(CH3)2、CH2BrCBr(CH3)2、CH2BrCH(CH3)CH2Br,
故答案为:CHBr2CH(CH3)2、CH2BrCBr(CH3)2、CH2BrCH(CH3)CH2Br.
点评 本题考查有机推断,是对有机化合物知识的综合考查,能较好的考查考生的思维能力,推断A的结构是本题的难点、易错点,难度中等.

练习册系列答案
相关题目
11.现有部分前36号元素的性质或原子结构如下表:
(1)写出R元素与同周期相邻元素的第一电离能由大到小的顺序,(用元素符号表示)N>O>C.
(2)S元素的常见化合价为-1,其基态原子的价电子排布图为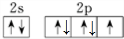
(3)T元素的原子N能层上电子数为2.
(4)X的电子排布图违背了能量最低原理.用X单质、碱金属盐及碱土金属盐等可以做成焰火.燃放时,焰火发出五颜六色的光,请用原子结构的知识解释发光的原因:电子从能量较高的轨道跃迁到能量较低的轨道时,以光的形式释放能量.
| 元素编号 | 元素性质或原子结构 |
| R | 基态原子的最外层有3个未成对电子,次外层有2个电子 |
| S | 单质能与水剧烈反应,所得溶液呈弱酸性 |
| T | 基态原子3d轨道上有1个电子 |
| X |  |
(2)S元素的常见化合价为-1,其基态原子的价电子排布图为

(3)T元素的原子N能层上电子数为2.
(4)X的电子排布图违背了能量最低原理.用X单质、碱金属盐及碱土金属盐等可以做成焰火.燃放时,焰火发出五颜六色的光,请用原子结构的知识解释发光的原因:电子从能量较高的轨道跃迁到能量较低的轨道时,以光的形式释放能量.
12.在一密闭容器中充入一定量的H2和N2,经测定反应开始后3s末的v(H2)=0.3mol•L-1•s-1,则3s末NH3的浓度为( )
| A. | 0.4 mol•L-1 | B. | 0.6 mol•L-1 | C. | 0.9 mol•L-1 | D. | 1.2 mol•L-1 |
16.下列热化学方程式能表示可燃物的燃烧热的是( )
| A. | H2(g)+Cl2(g)=2HCl(g)△H=-184.6kJ/mol | |
| B. | CH4(g)+2O2(g)=CO2(g)+2H2O(g)△H=-802.3kJ/mol | |
| C. | 2C8H18(g)+25O2(g)=16CO2(g)+18H2O(l)△H=-5518kJ/mol | |
| D. | CO(g)+$\frac{1}{2}$O2(g)=CO2(g)△H=-283kJ/mol |
13.长式周期表共有18个纵列,从左到右排为1~18列,即碱金属为第1列,稀有气体元素为第18列.按这种规定,下列说法正确的是( )
| A. | 第14列元素中未成对电子数是同周期元素中最多的 | |
| B. | 只有第2列的元素原子最外层电子排布为ns2 | |
| C. | 第四周期第8列元素是铁元素 | |
| D. | 第15列元素原子的价电子排布为ns2np5 |
10.利用甲烷燃料电池电解饱和食盐水制备漂白液,下列说法中不正确的是( )
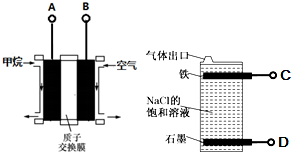

| A. | 燃料电池的A极连接电解池的C极 | |
| B. | A电极的电极反应式为:CH4-8e-+2H2O=CO2+8H+ | |
| C. | 燃料电池工作时H+移向左边 | |
| D. | 电解池总反应式为NaCl+H2O$\frac{\underline{\;电解\;}}{\;}$NaClO+H2↑ |
20.己知25℃,几种弱酸的电离平衡常数如表,电离平衡常数现有CH3COONa、NaClO、NaHCO3、Na2CO3、NaHSO3、Na2SO3六种盐溶液.
(1)比较等浓度的六种盐溶液中c(H+)的大小NaHSO3>CH3COONa>NaHCO3>Na2SO3>NaClO>Na2CO3;
(2)往六种盐溶液中分别通入少量SO2,请判断是否能反应,如果能,写出相应化学方程式SO2+H2O+2CH3COONa=2CH3COOH+Na2SO3、SO2+H2O+3NaClO=Na2SO3+2HClO+NaCl、SO2+2NaHCO3=Na2SO3+2CO2↑+H2O、SO2+H2O+Na2CO3=NaHCO3+NaHSO3、SO2+H2O+Na2SO3=2NaHSO3.
| 酸 | 电离平衡常数 |
| 醋酸 | Ka=1.75×10-5 |
| 次氯酸 | Ka1=2.98×10-8 |
| 碳酸 | Ka1=4.30×10-7 Ka2=5.61×10-11 |
| 亚硫酸 | Ka1=1.54×10-2 Ka2=1.02×10-7 |
(2)往六种盐溶液中分别通入少量SO2,请判断是否能反应,如果能,写出相应化学方程式SO2+H2O+2CH3COONa=2CH3COOH+Na2SO3、SO2+H2O+3NaClO=Na2SO3+2HClO+NaCl、SO2+2NaHCO3=Na2SO3+2CO2↑+H2O、SO2+H2O+Na2CO3=NaHCO3+NaHSO3、SO2+H2O+Na2SO3=2NaHSO3.
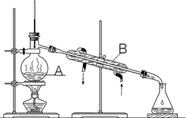 (1)指出图装置中A、B的名称
(1)指出图装置中A、B的名称