题目内容
16.茚是从煤油中提取的一种无色透明油状液体,不溶于水,可用于制造合成树脂.其结构简式为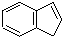 .下列关于茚的说法中不正确的是( )
.下列关于茚的说法中不正确的是( )| A. | 茚能使酸性高锰酸钾溶液褪色 | |
| B. | 茚能使溴的四氯化碳溶液褪色 | |
| C. | 1 mol茚只含有1 mol碳碳双键 | |
| D. | 茚中所有的原子均可能处在同一平面上 |
分析 由结构简式为 ,分子中含苯环和碳碳双键,结合苯及烯烃的性质来解答.
,分子中含苯环和碳碳双键,结合苯及烯烃的性质来解答.
解答 解:A.含碳碳双键,能使酸性高锰酸钾溶液褪色,故A正确;
B.含碳碳双键,能使溴的四氯化碳溶液褪色,故B正确;
C.只有1个碳碳双键,1 mol茚只含有1 mol碳碳双键,故C正确;
D.苯环及碳碳双键均平面结构,而含亚甲基为四面体结构,不可能所有原子共面,故D错误;
故选D.
点评 本题考查有机物的结构与性质,为高频考点,把握官能团与性质的关系为解答的关键,侧重分析与应用能力的考查,注意烯烃的性质,题目难度不大.

练习册系列答案
相关题目
7.铅、二氧化铅、氟硼酸(HBF4)电池是一种低温性能优良的电池,常用于军事和国防工业,其总反应方程式为Pb+PbO2+4HBF4$?_{充电}^{放电}$2Pb(BF4)2+2H2O[已知:HBF4、Pb(BF4)2均是易溶于水的强电解质].下列说法中不正确的是( )
| A. | 充电时,阳极附近溶液的pH增大 | |
| B. | 充电时,阴极的电极反应式为pb2++2e-═pb | |
| C. | 放电时,转移1mol电子时负极减少的质量为103.5g | |
| D. | 放电时,正极的电极反应式为PbO2+2e-+4H+═pb2++2H2O |
4.某学生配置0.1mol.L-1的NaOH溶液480mL,下列说法正确的是( )
| A. | 选用480 mL 容量瓶 | |
| B. | 把烧碱固体放在纸上称量 | |
| C. | 把称好的固体放入容量瓶中稀释至刻度线 | |
| D. | 定容时俯视容量瓶的刻度线浓度偏大 |
11.现有部分前36号元素的性质或原子结构如下表:
(1)写出R元素与同周期相邻元素的第一电离能由大到小的顺序,(用元素符号表示)N>O>C.
(2)S元素的常见化合价为-1,其基态原子的价电子排布图为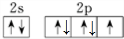
(3)T元素的原子N能层上电子数为2.
(4)X的电子排布图违背了能量最低原理.用X单质、碱金属盐及碱土金属盐等可以做成焰火.燃放时,焰火发出五颜六色的光,请用原子结构的知识解释发光的原因:电子从能量较高的轨道跃迁到能量较低的轨道时,以光的形式释放能量.
| 元素编号 | 元素性质或原子结构 |
| R | 基态原子的最外层有3个未成对电子,次外层有2个电子 |
| S | 单质能与水剧烈反应,所得溶液呈弱酸性 |
| T | 基态原子3d轨道上有1个电子 |
| X |  |
(2)S元素的常见化合价为-1,其基态原子的价电子排布图为

(3)T元素的原子N能层上电子数为2.
(4)X的电子排布图违背了能量最低原理.用X单质、碱金属盐及碱土金属盐等可以做成焰火.燃放时,焰火发出五颜六色的光,请用原子结构的知识解释发光的原因:电子从能量较高的轨道跃迁到能量较低的轨道时,以光的形式释放能量.
1.下面关于Na2CO3与NaHCO3的叙述错误的是( )
| A. | NaHCO3加热分解转化为Na2CO3 | |
| B. | 在水中的溶解度:Na2CO3比NaHCO3大 | |
| C. | 与同浓度的稀硫酸反应时,Na2CO3比NaHCO3剧烈 | |
| D. | NaHCO3能与NaOH反应,而Na2CO3不能 |
8.绿色植物中的维生素C具有明显的抗衰老作用,但易被空气氧化,某课外小组利用碘滴定法测某橙汁中维生素C的含量,其化学方程式为:
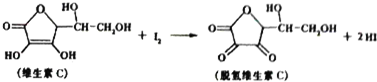
下列说法正确的是( )

下列说法正确的是( )
| A. | 脱氢维生素C的分子式为C6H7O6 | B. | 上述反应为氧化反应 | ||
| C. | 滴定时反应剧烈振荡锥形瓶 | D. | 滴定时不可以用淀粉溶液作指示剂 |
 金属镍及其化合物在合金材料以及催化剂等方面应用广泛.根据要求回答下列问题:
金属镍及其化合物在合金材料以及催化剂等方面应用广泛.根据要求回答下列问题: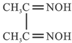 )作用生成腥红色配合物沉淀A.
)作用生成腥红色配合物沉淀A.